Химия: уроки, тесты, задания.
Первоначальные химические понятия и теоретические представления
-
Предмет химии
-
Физические тела и вещества
-
Чистые вещества и смеси
-
Разделение смесей. Методы очистки веществ
-
Атомы и молекулы
-
Химические элементы. Знаки химических элементов
-
Закон постоянства состава
-
Химические формулы
-
Простые и сложные вещества
-
Валентность. Степень окисления. Составление формул по валентностям и степеням окисления
-
Физические и химические явления
-
Признаки и условия протекания химических реакций
-
Закон сохранения массы веществ
-
Уравнения химических реакций
Классы неорганических веществ
-
Классификация веществ
-
Металлы
-
Неметаллы
-
Оксиды
-
Основания
-
Кислоты
-
Амфотерные гидроксиды
-
Соли
-
Взаимосвязь между классами неорганических веществ
Периодический закон и строение атомов
-
Периодический закон
-
Периодическая система
-
Строение ядра атома
-
Строение электронной оболочки атома
-
Периодическая таблица и закономерности изменения свойств химических элементов
Строение вещества
-
Электроотрицательность химических элементов
-
Типы химической связи
-
Ионная связь
-
Ковалентная связь
-
Металлическая связь
-
Аморфные и кристаллические вещества
-
Кристаллические решётки
Окислительно-восстановительные реакции
-
Степень окисления
-
Окислители и восстановители, окисление и восстановление
Растворы
-
Состав растворов
-
Растворение. Растворимость
-
Электролиты и неэлектролиты
-
Электролитическая диссоциация кислот, оснований и солей
-
Свойства ионов
-
Среда растворов. Индикаторы
-
Реакции ионного обмена. Реакция нейтрализации
Классификация химических реакций и закономерности их протекания
-
Классификация химических реакций по числу и составу вступивших в реакцию и образовавшихся веществ
-
Классификация химических реакций по тепловому эффекту
-
Классификация химических реакций, ОВР
-
Скорость протекания химической реакции. Катализаторы
Химия неметаллов
-
Водород
-
Кислород
-
Вода
-
Галогены. Хлор и его соединения
-
Сера и её соединения
-
Азот и его соединения
-
Фосфор и его соединения
-
Углерод и его соединения
-
Кремний и его соединения
Химия металлов
-
Щелочные металлы и их соединения
-
Щелочноземельные металлы и их соединения
-
Алюминий и его соединения
-
Железо и его соединения
Органические вещества
-
Состав и строение органических веществ
-
Углеводороды. Полимеры
-
Спирты
-
Карбоновые кислоты
-
Жиры
-
Углеводы
-
Белки
Человек в мире веществ, материалов и химических реакций
-
Природные источники углеводородов
-
Химия и пища. Химия и здоровье
Методы исследования в химии
-
Методы научного познания. Химический эксперимент
-
Получение, собирание и распознавание газов
-
Обнаружение ионов
Расчётные задачи по химии
-
Физические величины
-
Относительная атомная и молекулярная массы. Вычисление относительной молекулярной массы вещества
-
Количество вещества
-
Вычисление молярной массы вещества
-
Вычисление количества вещества
-
Вычисление массовой доли элемента в химическом соединении
-
Установление простейшей формулы вещества по массовым долям элементов
-
Простейшие вычисления по уравнениям химических реакций
-
Вычисления по уравнениям реакций, если исходное вещество содержит определенную долю примесей
-
Вычисление массовой доли вещества в растворе
-
Вычисления, связанные с приготовлением растворов с заданной массовой долей растворённого вещества
-
Комбинированные задачи
Класс заполнен на 100 %
www.yaklass.ru
Беря в помощники Vshkole, химия в 8 классе изучается легко и просто
Химия является одним из самых сложных школьных предметов, так как содержит большой объем материала и заданий к нему. Но все же, эта дисциплина играет огромную роль в жизни каждого школьника, так как помогает ему познавать мир вокруг себя и знакомит его с главными составляющими нашего существования. Труднее всего приходится восьмиклассникам, которые должны изучать и органическую, и неорганическую химию. Современные школьники нашли способ, как быстро и без затруднений справляться с домашней работой, взяв себе в союзники — готовые домашние задания.
<p «>Благодаря решебникам, химия 8 класс становится любимым предметом учеников. Все дело в том, что ГДЗ оказывают сильное положительное влияние, как на успеваемость, так и на усвоение знаний. Подросток начинает получать только высокие оценки за самостоятельно сделанную домашнюю работу, которая составляет почти половину общих отметок. Это происходит из-за наличия в готовых домашних заданиях правильных ответов на различные упражнения, поэтому ученик 8 класса всегда сможет проверить свою работу и исправить ошибки, если те были допущены. Теперь, сдавая свою рабочую тетрадь, ученик будет уверен, что она выполнена на 100% верно.
Улучшение усвоения знаний происходит с помощью специальных элементов ГДЗ. В каждом справочнике такого типа предлагаются подробные и поэтапные решения заданий. Просматривая их, школьник без проблем сможет разобраться с алгоритмом применения того или иного правила на практике. Теперь выполнить задание, которое по типу совпадает с уже просмотренным, ученику будет легко.
Также не стоит забывать о таком компоненте готовых домашних заданий за 8 класс как объяснения. Эти лаконичные заметки отлично поспособствуют лучшему пониманию учеником материала и обеспечат его запоминание на длительный период.
Приступая к выполнению домашней работы по химии, перед школьниками и их родителями стоит серьезная задача – найти качественные решебники по данному предмету. Взявшись за ее выполнение, современные ученики даже не думают посещать рынки книги, ведь главным для них источником учебных материалов является сеть интернет.
<p «>Среди множества образовательных порталов, предлагающих ГДЗ по химии, выгодно отличается сайт Вшколе. Этот интернет ресурс не просто предоставляет лучшие учебные книги (готовые домашние задания, учебники), но не скрывает к ним доступ. То есть, каждый желающий в любое время может просматривать необходимую ему информацию абсолютно бесплатно и без каких-либо регистраций.
Вшколе станет Вашим секретом, обеспечивающим высокие отметки за выполнение домашней работы и хорошее знание химии за 8 класс. Учитесь с удовольствием вместе с надежными ГДЗ!
zadachi-po-khimii.ru
Предмет химии. Видеоурок. Химия 8 Класс
Химия – это наука о веществах, их свойствах и превращениях друг в друга.
Все, что нас окружает, – люди, животные, растения, горы, моря, предметы – имеет непосредственное отношение к химии. Окружающие нас предметы и объекты называют физическими телами. Тела состоят из множества различных веществ. К настоящему моменту известно около 15 миллионов веществ, и это далеко не предел!
Гвоздь – это тело, состоящее из вещества – железа. Кусок гранита – это тоже тело, состоящее из нескольких веществ – кварца, слюды и полевого шпата. Рис. 1.
Рис. 1. Гранит и составляющие его вещества
Одни и те же тела часто изготавливают из разных веществ. Например, проволока может быть медной, железной, алюминиевой. И наоборот, из одного и того же вещества могут быть изготовлены различные тела: из стекла сделаны разные виды посуды, вазы и т. д.
Запомните! Каждое тело состоит из какого-либо вещества!
Физические свойства веществ
Каждое вещество характеризуется определенными свойствами.
Свойства вещества – это признаки, по которым вещества отличаются друг от друга или сходны между собой.
К физическим свойствам вещества относятся его
- плотность,
- агрегатное состояние,
- цвет,
- температуры плавления и кипения,
- электро- и теплопроводность.
Одна из задач химии – это изучение веществ, их свойств и прогнозирование использования веществ в промышленности, сельском хозяйстве и медицине.
Например, вещество алюминий – это металл серебристо-белого цвета. Сравнительно легкий (его плотность составляет 2,7 г/см3), плавится при температуре 600 °С. Алюминий очень пластичен и обладает хорошей электропроводностью. Из-за легкости алюминий в виде сплавов используют в самолето- и ракетостроении. Его также используют для изготовления электрических проводов и предметов быта. Рис. 2.
Рис. 2. Алюминий и изделия из него
Физические явления
Кроме физических свойств, каждое вещество обладает способностью к превращению. Что же такое превращение веществ?
Представьте, что мы нагрели воду и она испарилась. Произошло ли при этом превращение вещества? Нет, испарение воды – это физическое явление. Водяной пар – это химическое вещество вода, только не в жидком, а газообразном агрегатном состоянии.
Физические явления – это явления, при которых данные вещества не превращаются в другие, а только изменяется их агрегатное состояние или форма.
Химические явления или химические реакции
Возьмем другой пример – ржавление железа. Железо ржавеет при взаимодействии с водой и кислородом. Ржавчина – хрупкое вещество бурого цвета. Таким образом, происходит превращение веществ – железа, кислорода и воды – в ржавчину. Это явление относится к химическим. Химические явления иначе называют химическими реакциями.
Химические явления или химические реакции – это явления, при которых из данных веществ образуются другие.
Вещества, вступающие в химическую реакцию (в рассмотренном примере – это железо, кислород и вода), называют исходными веществами.
Вещества, получающиеся в результате реакции (в данном случае – ржавчина), называют продуктами реакции.
Вывод
При физическом явлении изменения вещества не происходит, а изменяется лишь его агрегатное состояние или форма. В результате химической реакции происходит превращение исходных веществ в продукты реакции. Рис. 3.
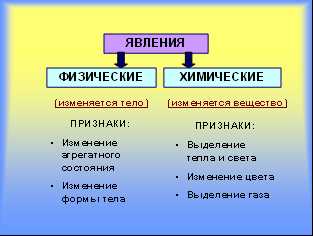
Рис. 3. Классификация явлений
Признаки химической реакции
О протекании химического превращения можно судить по следующим признакам:
- выпадение осадка,
- выделение газа,
- изменение цвета,
- выделение или поглощение тепла и другим.
Есть химические превращения, при которых не происходит проявления признаков реакции. Более того, ряд перечисленных признаков может соответствовать и физическим процессам. Стоит открыть, например, бутылку с газированным напитком, как из нее с шипением выделится углекислый газ, который был растворен в воде под большим давлением.
При охлаждении насыщенного раствора растворенное вещество часто выпадает в осадок. Такое явление называют кристаллизацией. Кристаллизация не сопровождается превращением вещества, т. е. относится к физическим явлениям.
Подведение итога урока
Химия – это наука о веществах, химических реакциях и их применении.
Химические знания помогают бороться с различными болезнями человека, животных и растений. Изучая свойства веществ, составляющих неживую природу, люди учатся бережно и грамотно ее использовать.
Список литературы
- Сборник задач и упражнений по химии: 8-й класс: к учебнику П.А. Оржековского и др. «Химия, 8 класс» / П.А. Оржековский, Н.А. Титов, Ф.Ф. Гегеле. – М.: АСТ: Астрель, 2006. (с. 8–10)
- Химия: 8-й класс: учеб. для общеобр. учреждений / П.А. Оржековский, Л.М. Мещерякова, Л.С. Понтак. М.: АСТ: Астрель, 2005.(с. 7–10)
- Химия: неорг. химия: учеб. для 8 кл. общеобр. учреждений / Г.Е. Рудзитис, ФюГю Фельдман. – М.: Просвещение, ОАО «Московские учебники», 2009. (§1)
- Энциклопедия для детей. Том 17. Химия / Глав. ред.В.А. Володин, вед. науч. ред. И. Леенсон. – М.: Аванта+, 2003. (с. 8–36)
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
- Единая коллекция цифровых образовательных ресурсов (видеоопыты по теме) (Источник).
- Электронная версия журнала «Химия и жизнь» (Источник).
Домашнее задание
№№ 1–3, 5–7 из Сборника задач и упражнений по химии: 8-й класс: к учебнику П.А. Оржековского и др. «Химия, 8 класс» / П.А. Оржековский, Н.А. Титов, Ф.Ф. Гегеле. – М.: АСТ: Астрель, 2006.
interneturok.ru
|
№ п/п |
Тема урока |
Кол-во часов |
Тип урока |
Требования к уровню подготовки обучающихся |
Основные понятия |
Дата проведения план/факт |
|
Тема 1. Введение. Первоначальные химические понятия (6 часов) |
||||||
|
1. |
Предмет химии |
1 |
урок формирования новых знаний |
Знать предмет изучения химии; понимать логическую связь между понятиями «атом», «молекула», «вещество», «тело»; определять элемент как совокупность атомов определенного вида. |
Наблюдение, эксперимент, моделирование. |
|
|
2. |
Вещества |
1 |
урок формирования новых знаний |
Знать определение важнейших понятий: простые и сложные вещества, химический элемент, атом, молекула. Различать понятия «вещество» и «тело», «простое вещество» и «химический элемент» |
Простые и сложные вещества, свойства веществ, химический элемент, формы существования ХЭ, атомы и молекулы. |
|
|
3. |
Превращения веществ. Роль химии в жизни человека |
1 |
комбинированный урок |
Уметь отличать химические реакции от физических явлений. Использовать приобретенные знания для безопасного обращения с веществами и материалами, экологически грамотного поведения в окружающей среде, оценки влияния химического загрязнения окружающей среды на организм человека |
Химические явления, или реакции, физические явления. |
|
|
4. |
Периодическая система химических элементов. Знаки химических элементов |
1 |
комбинированный урок |
Уметь определять положение химического элемента в ПСХЭ. Уметь называть химические элементы. Знать знаки первых 20 химических элементов. |
ПСХЭ Д.И. Менделеева, периоды большие и малые, группы и подгруппы, символы химических элементов. |
|
|
5. |
Химические формулы. Относительная атомная и молекулярная массы |
1 |
комбинированный урок |
Знать определение химической формулы вещества, формулировку закона постоянства состава. Понимать и записывать химические формулы веществ. Определять состав веществ по химической формуле, принадлежность к простым и сложным веществам. |
Химическая формула, индексы и коэффициенты, относительная атомная масса, относительная молекулярная масса, массовая доля элемента в веществе. |
|
|
6. |
Расчеты по химической формуле вещества |
1 |
комбинированный урок |
Уметь вычислять массовую долю химического элемента по формуле соединения |
Химическая формула, индексы и коэффициенты, относительная атомная масса, относительная молекулярная масса, массовая доля элемента в веществе. |
|
|
Тема 2. Атомы химических элементов (10 часов) |
||||||
|
7. |
Основные сведения о строении атомов |
1 |
изучение и первичное закрепление знаний |
Уметь объяснять физический смысл атомного (порядкового) номера химического элемента |
Строение атома, строение ядра, сканирующий микроскоп, нанотехнологии. |
|
|
8. |
Ядерные реакции. Изотопы. |
1 |
комбинированный урок |
Знать определение понятия «химический элемент» |
Изотопы, ядерные процессы, изотопы водорода. |
|
|
9. |
Строение электронных оболочек атомов |
1 |
изучение и первичное закрепление знаний |
Уметь объяснять физический смысл номера группы и периода, составлять схемы строения атомов первых 20 элементов периодической системы химических элементов Д.И.Менделеева |
Строение электронных оболочек атомов элементов №1-20 в периодической таблице. |
|
|
10. |
Периодический закон и периодическая система Химических элементов Д.И.Менделеева |
1 |
комбинированный урок |
Знать формулировку периодического закона. Уметь объяснять закономерности изменения свойств элементов в пределах малых периодов и главных подгрупп. Уметь характеризовать химические элементы (от H до Ca) на основе их положения в ПСХЭ и особенностей строения их атомов |
ПЗ и ПСХЭ. Группы и периоды, строение атома, простые вещества. |
|
|
11. |
Ионная связь |
1 |
комбинированный урок |
Знать определение понятий: «химическая связь», «ион», «ионная связь». Уметь определять тип химической связи (ионная) в соединениях. |
Ионная химическая связь. |
|
|
12. |
Ковалентная неполярная связь |
1 |
комбинированный урок |
Уметь определять тип химической связи (ковалентная неполярная) в соединениях |
Ковалентная неполярная химическая связь, длина связи. |
|
|
13. |
Ковалентная полярная связь |
1 |
комбинированный урок |
Уметь определять тип химической связи (ковалентная полярная) в соединениях |
Ковалентная полярная химическая связь, электроотрицательность, валентность,. |
|
|
14. |
Металлическая связь |
1 |
комбинированный урок |
Знать определение металлической связи, объяснять свойства металлов, исходя из типа химической связи, находить черты сходства и различия её с ковалентной и ионной связью. |
Металлическая связь, атом-ион, обобществлённые электроны. |
|
|
15. |
Повторение |
1 |
урок обобщения, систематизации и коррекции знаний |
Знать определения видов химической связи. Уметь определять в веществах химическую связь. |
|
|
|
16. |
Контрольная работа №1 по темам: «Первоначальные химические понятия», «Атомы химических элементов» |
1 |
урок контроля |
Знать строение атомов, виды химической связи. Уметь определять в веществах химическую связь. |
|
|
|
Тема 3. Простые вещества (7 часов) |
||||||
|
17. |
Простые вещества — металлы |
1 |
изучение и первичное закрепление знаний |
Знать общие физические свойства металлов. Характеризовать связь между составом, строением и свойствами металлов. |
Простые вещества-металлы, физические свойства металлов: ковкость, пластичность, тягучесть, твёрдость, температура кипения, металлический блеск, электро- и теплопроводность. |
|
|
18. |
Простые вещества — неметаллы |
1 |
изучение и первичное закрепление знаний |
Уметь характеризовать физические свойства неметаллов. Понимать связь между составом, строением и свойствами неметаллов. |
Благородные газы, аллотропия и аллотропные видоизменения, кислород и озон, алмаз и графит, фосфор красный и белый, белое и серое олово. |
|
|
19. |
Количество вещества. Молярная масса |
1 |
комбинированный урок |
Знать определение понятий «моль», «молярная масса». Уметь вычислять молярную массу по формуле соединения, массу вещества и число частиц по известному количеству вещества (и обратные задачи). |
Количество вещества и единица его измерения: моль, моль, кмоль. постоянная Авогадро. Молярная масса. |
|
|
20. |
Молярный объем газов. Закон Авогадро |
1 |
комбинированный урок |
Знать определение молярного объема газов. Уметь вычислять объем газа по его количеству, массу определенного объема или числа молекул газа (и обратные задачи) |
Понятие молярный объем газов, нормальные условия. |
|
|
21. |
Решение задач с использованием понятий «количество вещества», «молярная масса», «Молярный объем», «число Авогадро» |
1 |
урок-упражнение |
Уметь вычислять молярную массу по формуле соединения, массу вещества и число частиц по известному количеству вещества; объем газа по его количеству, массу определенного объема или числа молекул газа (и обратные задачи) |
Решение задач и упражнений с использованием понятий темы. |
|
|
22. |
Решение задач с использованием понятий «количество вещества», «молярная масса», «Молярный объем», «число Авогадро» |
1 |
урок-упражнение |
Уметь вычислять молярную массу по формуле соединения, массу вещества и число частиц по известному количеству вещества; объем газа по его количеству, массу определенного объема или числа молекул газа (и обратные задачи) |
Решение задач и упражнений с использованием понятий темы. |
|
|
23. |
Повторение по теме «Простые вещества» |
1 |
урок обобщения, систематизации и коррекции знаний |
Знать определение основных терминов темы. Уметь производить расчеты. |
|
|
|
Тема 4. Соединения химических элементов (14 часов) |
||||||
|
24. |
Степень окисления и валентность |
1 |
изучение и первичное закрепление знаний |
Уметь определять валентность и степень окисления элементов в бинарных соединениях, составлять формулы соединений по степени окисления, называть бинарные соединения. |
Бинарные соединения, степень окисления, составление формул бинарных соединений. |
|
|
25. |
Важнейшие классы бинарных соединений – оксиды и летучие водородные соединения |
1 |
комбинированный урок |
Уметь определять принадлежность вещества к классу оксидов, называть его, составлять формулы оксидов. |
Оксиды, вода, углекислый газ, гидриды, летучие водородные соединения. |
|
|
26. |
Основания |
1 |
комбинированный урок |
Уметь определять принадлежность вещества к классу оснований, называть его, составлять формулы оснований. Знать качественную реакцию на углекислый газ, на распознавание щелочей. |
Гидроксид-ион, основания, качественные реакции, индикаторы: лакмус, метиловый оранжевый, фенолфталеин. |
|
|
27. |
Кислоты |
1 |
комбинированный урок |
Уметь определять принадлежность вещества к классу кислот, знать формулы и названия кислот. Знать качественную реакцию на распознавание кислот. |
Кислоты кислородсодержащие и бескислородные, кислотные остатки и основность кислот, сложные и простые ионы, универсальный индикатор. |
|
|
28. |
Соли |
1 |
комбинированный урок |
Уметь определять принадлежность вещества к классу солей, составлять формулы солей, называть их. |
Соли, номенклатура солей, составление формул солей. |
|
|
29. |
Кристаллические решетки |
1 |
изучение и первичное закрепление знаний |
Уметь характеризовать и объяснять свойства веществ на основании вида химической связи и типа кристаллической решетки. |
Твёрдое, жидкое и газообразное состояние вещества, кристаллические решётки: ионные, атомные, молекулярные и металлические. |
|
|
30. |
Чистые вещества и смеси |
1 |
изучение и первичное закрепление знаний |
Понимать отличие между смесью и индивидуальным веществом, понимать, что абсолютно чистых веществ нет, уметь объяснять, зачем нужен химический анализ, знать отличие дистиллированной воды от водопроводной |
Чистые вещества и смеси, химический анализ. |
|
|
31. |
Массовая и объемная доли компонентов смеси (раствора) |
1 |
комбинированный урок |
Уметь вычислять массовую долю вещества в растворе. |
Массовая доля, проба золота, объёмная доля и объёмный состав воздуха. |
|
|
32. |
Решение расчетных задач на нахождение объемной и массовой долей смеси |
1 |
урок-упражнение |
Уметь вычислять массовую долю вещества в растворе. |
|
|
|
33. |
Приёмы обращения с лабораторным оборудованием. Практическая работа № 1 |
1 |
практическая работа |
Уметь обращаться с химической посудой и лабораторным оборудованием. |
Правила работы в школьной лаборатории. Лабораторная посуда и оборудование, правила безопасности. |
|
|
34. |
Наблюдение за изменениями, происходящими с горящей свечой, и их описание. Практическая работа № 2 |
1 |
практическая работа |
Знать правила техники безопасности при работе в школьной лаборатории. |
Правила работы в школьной лаборатории. Лабораторная посуда и оборудование, правила безопасности. |
|
|
35. |
Приготовление раствора сахара и расчёт его массовой доли в растворе. Практическая работа № 3 |
1 |
практическая работа |
Уметь готовить растворы заданной концентрации. |
Взвешивание и приготовление раствора. |
|
|
36. |
Повторение по теме: «Соединения химических элементов» |
1 |
урок обобщения, систематизации и коррекции знаний |
Знать определение основных терминов темы. Уметь производить расчеты. |
|
|
|
37. |
Контрольная работа №2 по теме «Соединения химических элементов» |
1 |
урок контроля |
Знать определение основных терминов темы. Уметь производить расчеты. |
|
|
|
Тема 5. Изменения, происходящие с веществами (13 часов) |
||||||
|
38. |
Физические явления |
1 |
изучение и первичное закрепление знаний |
Знать способы разделения смесей. |
Дистилляция, дистиллированная вода, кристаллизация, фильтрование, возгонка, отстаивание, делительная воронка, центрифугирование. |
|
|
39. |
Очистка загрязненной поваренной соли. Практическая работа № 4 |
1 |
практическая работа |
Уметь обращаться с химической посудой и лабораторным оборудованием при проведении опытов с целью очистки загрязненной поваренной соли. |
Правила работы в школьной лаборатории. Лабораторная посуда и оборудование, правила безопасности. |
|
|
40. |
Химические реакции |
1 |
комбинированный урок |
Знать определение понятия «химическая реакция», признаки и условия течения химических реакций, типы реакций по поглощению или выделению энергии. |
Признаки химических реакций, условия течения химических реакций, реакции экзо- и эндотермические, реакция горения. |
|
|
41. |
Химические уравнения |
1 |
комбинированный урок |
Знать определение понятия «химическая реакция». Уметь составлять уравнения химических реакций на основе закона сохранения массы веществ. |
Химические уравнения, правила подбора коэффициентов в уравнениях реакций. |
|
|
42. |
Расчеты по химическим уравнениям |
1 |
комбинированный урок |
Уметь вычислять по химическим уравнениям массу, объем или количество одного из продуктов реакции по массе исходного вещества и вещества, содержащего определенную долю примесей |
Единицы важнейших величин, алгоритм вычисления по уравнению реакции. |
|
|
43. |
Расчеты по химическим уравнениям |
1 |
урок-упражнение |
Уметь вычислять по химическим уравнениям массу, объем или количество одного из продуктов реакции по массе исходного вещества и вещества, содержащего определенную долю примесей |
Единицы важнейших величин, алгоритм вычисления по уравнению реакции. |
|
|
44. |
Реакции разложения |
1 |
комбинированный урок |
Уметь отличать реакции разложения от других типов реакций, составлять уравнения реакций данного типа. |
Реакции разложения, скорость химической реакции, катализаторы, ферменты. |
|
|
45. |
Реакции соединения |
1 |
комбинированный урок |
Уметь отличать реакции соединения от других типов реакций, составлять уравнения реакций данного типа. |
Реакции соединения, каталитические и некаталитические реакции, цепочки превращения, обратимые и необратимые реакции. |
|
|
46. |
Реакции замещения |
1 |
комбинированный урок |
Уметь отличать реакции замещения от других типов реакций, знать условия течения и уметь составлять уравнения реакций взаимодействия металлов с растворами кислот и солей, используя ряд активности металлов |
Реакции замещения, ряд активности металлов. |
|
|
47. |
Реакции обмена |
1 |
комбинированный урок |
Уметь отличать реакции обмена от других типов реакций, составлять уравнения реакций данного типа, определять возможность протекания реакций обмена в растворах до конца. |
Реакции обмена, реакции нейтрализации, условия протекания реакций обмена в растворах до конца |
|
|
48. |
Типы химических реакций на примере свойств воды |
1 |
комбинированный урок |
Уметь составлять уравнения реакций, характеризующих химические свойства воды, определять типы химических реакций |
Электролиз, фотолиз, фотосинтез, щелочные и щёлочноземельные металлы, гидролиз. |
|
|
49. |
||||||
xn--j1ahfl.xn--p1ai