Конспект урока по химии на тему «Кислород» (9 класс)
Конспект урока
-
9 класс
-
Тема урока: Кислород
-
Цель: Систематизация и расширение знаний учащихся о кислороде, как простом веществе.
Задачи:
О:
— систематизировать, обобщить и углубить знания учащихся о химическом элементе кислороде,о простых
веществах кислороде и озоне,о его химических свойствах и способах получения кислорода;
— познакомить учащихся с нахождением кислорода в природе и его применением;
В:
— продолжить формирование научной картины мира;
— осуществить экологическое воспитание;
— волеологическое воспитание.
Р:
— развить у учащихся умения анализировать, сравнивать, обобщать учебный материал;
— развить познавательные умения слушать, выделять главное, выдвигать гипотезы, составлять план;
-
Оборудование и материалы: доска, мел, интерактивная доска, ПСХЭ Д.
 И. Менделеева, раздаточный материал,демонстрационный штатив с пробирками, лучинка, спички, перекись водорода, оксид марганца (IV).
И. Менделеева, раздаточный материал,демонстрационный штатив с пробирками, лучинка, спички, перекись водорода, оксид марганца (IV). -
Тип урока: урок открытия нового знания.
-
Методы и методические приемы: словесные (объяснение с элементами беседы), словесно-наглядные (химический эксперимент, демонстрация презентации)
-
Литературадля учителя:
-
Габриелян, О. С. Химия. 9 класс : учебник / О. С. Габриелян. – 2-е изд., стереотип. – М. : Дрофа, 2014. – 319, [1] с. : ил.
-
Рабочие программы. Химия. 7 – 9 : учебно-методическое пособие / сост. Т. Д. Гамбурцева. – 2-е изд., перераб. – М. : Дрофа, 2013. – 159, [1] с.
Литература для ученика:
-
Габриелян, О. С. Химия. 9 класс : учебник / О. С. Габриелян. – 2-е изд., стереотип. – М. : Дрофа, 2014. – 319, [1] с. : ил.
-
Габриелян, О. С. Химия. 9 кл. : рабочая тетрадь к учебнику О.С. Габриеляна «Химия. 9 класс» / О. С. Габриелян, С.
 А. Сладков. – 2-е изд., стереотип. – М. : Дрофа, 2014. – 221, [3] с, : ил.
А. Сладков. – 2-е изд., стереотип. – М. : Дрофа, 2014. – 221, [3] с, : ил.
-
Структура урока с хронологией
-
Организационный момент – 1 мин.
-
Подготовка к изучению нового материала – 4 мин.
-
Сообщение темы, цели, задач урока, мотивация учебной деятельности школьников – 3 мин.
-
Ознакомление с новым материалом – 20 мин.
-
Первичное осмысление и применение изученного материала – 10 мин.
-
Подведение итогов урока – 3 мин.
-
Сообщение домашнего задания и инструктаж – 4 мин.
-
Ход урока:
-
Основная часть
В чем горят дрова и газ,
Фосфор, водород, алмаз?
Дышит чем любой из нас
Каждый миг и каждый час?
Без чего мертва природа?
Правильно без …(слайд 1).
И так тема нашего сегодняшнего урока «Кислород»
Давайте вспомним, что вы знаете о кислороде?
Какими физическими свойствами обладает кислород?
Назовите аллотропные модификации кислорода?
Кто открыл кислород?
И так цель нашего урока:Систематизация и расширение знаний учащихся о кислороде
План урока:
-
Положение кислорода в ПСХЭ Д.
 И. Менделеева
И. Менделеева -
Химические свойства кислорода
-
Применение и роль кислорода в природе
Давайте посмотрим на ПСХЭ Д.И. Менделеева и охарактеризуем кислород (слайд 2).
С некоторыми аспектами химии кислорода вы уже частично знакомы. Получение кислорода из пероксида водорода и перманганата калия (слайд 3).
Какими методами собирают кислород (слайд 4)?
В начале урока мы вспоминали ученых, которые открыли кислород. И так, кислород открыли и впервые получили почти одновременно два выдающихся химика XVIII в. – швед К. Шееле путём нагревания селитры (слайды 5, 6) и англичанин Дж. Пристли при нагревании оксида ртути (слайд 7). Название этому элементу дал великий французский химик А. Лавуазье(слайд 8).
Кислород – самый распространенный элемент на нашей планете (слайд 9). Он входит в состав гидросферы (89%), атмосферы по объему (23%), по массе (21%), в состав литосферы (слайд 10).
Также вы хорошо знакомы с аллотропией кислорода. Какую аллотропную модификацию имеет кислород?
Какую аллотропную модификацию имеет кислород?
Заполните сравнительную таблицу (слайд 11).
Мы с вами повторили физические свойства кислорода. А как вы думаете какие еще есть свойства у кислорода?
Конечно, химичнеские.
Рассмотрим химические свойства кислорода
Кислород взаимодействует почти со всеми простыми веществами, кроме галогенов, благородных газов, золота и платиновых металлов. Например энергично реагируют с Ме: щелочными, образуя оксид с литием Li2O, или например пероксиды, с железом, образуя железную окалину Fe3O4.
Li+O2→ Li2O,
2Na+O2→Na2O2,
3Fe+2O2→Fe3O4
Реакции металлов и неметаллов с кислородом протекают с выделение теплоты, реакции идут при нагревании.
S+O2→SO2+Q,
4P+5O2→2P2O5+Q,
C+O2→CO2+Q.
Почти все реакции с кислородом эндотермические, но исключение составляет взаимодействие азота с кислородом: это эндотермическая реакция, протекающая при температуре выше 2000 градусов или при электрическом разряде:
N2+O2↔2NO – Q.
Кислород энергично окисляет не только простые, но и многие сложные вещества, при этом образуются оксиды элементов, из которых они построены:
CH4+2O2=2H2O+CO2,
2H2S+3O2=2SO2+2H2O.
Запишите все уравнения реакции в тетрадь.
Кислород участвует и в процессах дыхания. Медленное окисление пищи в нашем организме является источником энергии, за счет которой живет организм. Как вы думаете, что такое реакция окисления?
Вот и в нашем организме кислород доставляется гемоглобином крови, который способен образовываться с ним непрочное соединение уже при комнатной температуре. Окисленный гемоглобин доставляет во все ткани и клетки организма кислород, который окисляет белки, жиры и углеводы, образуя при этом оксид углерода (IV) и воду и освобождая энергию, необходимую для деятельности человека (слайд 12).
Как вы думаете, ребята растения дышат?
Растения также поглощают атмосферный кислород. Но если в темноте идет только процесс поглощения растениями кислорода, то на свету протекает еще один противоположный ему процесс, в результате которого растения поглощают углекислый газ и выделяют кислород. Как называется этот процесс? (слайд 13)
Напиши уравнение реакции фотосинтеза?
Содержание свободного кислорода Земли сохраняется благодаря зелёным растениям, хотя изначально атмосфера нашей планеты была другой. (стр 184, рис 112.)
Круговорот кислорода в природе (слайд 14).
Кислород широко используется и в быту. Как же его получают?
Именно сейчас я вам продемонстрирую опыт получение и распознавание кислорода. Для этого нам понадобится демонстрационный штатив и 2 демонстрационные пробирки. Наливаем в каждую по 5-10 мл раствора пероксида водорода. В первую пробирку добавляем на кончике шпателя оксид марганца (IV). Что вы наблюдаете? Как вы думаете, какой газ выделяется? Как доказать наличие кислорода в сосуде?
Доказываем наличие кислорода. Какую роль играет в этой реакции оксид марганца (IV)?
Какую роль играет в этой реакции оксид марганца (IV)?
Запишите наблюдение и вывод в тетрадь.
Давайте вспомним, где применяют кислород:
в металлургии и химической промышленности, для сварки и резки металлов, для жизнеобеспечения на подводных и космических кораблях, при работе водолазов, пожарных, в медицине – кислородные подушки (слайд 15).
Отвечают на вопрос.
Кислорода
С помощью приема «Кластер»
Формулируют цель урока.
Дают характеристику элемента кислорода по ПСХЭ Д.И. Менделеева.
2 период, VI А группа, неМе, атомная масса 16.
Отвечают на вопрос.
Методом вытеснения воды и воздуха.
Пристли, Шееле и Лавуазье.
Внимательно слушают учителя
Озон
Отвечают на вопрос.
Химические.
Слушают учителя и списывают уравнение химических реакций с доски в тетрадь.
Записывают уравнения реакции в тетрадь
Внимательно прослушивают материал
Реакции окисления – это такие реакции, которые протекают с участием кислорода.
Отвечают на вопрос.
Растения дышат.
Фотосинтез.
квант света
C6H12O6+6O2→6CO2+6H2O
Отвечают на вопрос.
Разложением пероксида водорода
Наблюдают за ходом проведения эксперимента.
Анализируют, делают выводы.
В первой пробирке идет бурное выделение пузырьков газа.
Кислород.
Тлеющая лучинка – ярко вспыхивает.
Роль катализатора.
Записывают наблюдение и вывод в тетрадь
Вывод: Кислород получают разложением пероксида водорода.
В металлургии, в медицине, Для сварки и резки металлов.
Беседа
Беседа
Объяснение с элементами беседы
Объяснение с частичным конспектированием
Объяснение
Беседа
Демонстрационный эксперимент
Беседа
III Заключительный этап
Закрепление изученного материала
Тестовые задания.
1. Какой газ образуется в результате фотосинтеза?
а) азот
б) кислород
в) углекислый газ.
2.Фосфор поместили в пробирку с кислородом, что образуется в результате реакции? Напишите уравнение химической реакции?
3. Фамилия английского ученого, получившего кислород разложением оксида ртути (II)?
а) А. Лавуазье
б) К. Шееле
в) Дж. Пристли
4. Вещества, ускоряющие химическую реакцию?
а) катализаторы
б) ингибиторы
5. Запишите уравнения химических реакций кислорода с азотом, с калием, с алюминием.
6. Самый распространенный химический элемент на Земле?
а) кислород
б) водород
в) кремний
Рефлексия «Синквейн» (слайд16).
Домашнее задание §25, стр. 180-188, задание 1, 8 (слайд 17).
Работают с раздаточным материалом
1. Какой газ образуется в результате фотосинтеза?
а) азот
б) кислород
в) углекислый газ.
2. Фосфор поместили в пробирку с кислородом, что образуется в результате реакции?Напишите уравнение химической реакции?
Фосфор поместили в пробирку с кислородом, что образуется в результате реакции?Напишите уравнение химической реакции?
Оксид фосфора (V), 4P+5O2→2P2O5+Q
3.Фамилия английского ученого, получившего кислород разложением оксида ртути (II) ?
а) А. Лавуазье
б) К. Шееле
в) Дж. Пристли
4. Вещества, ускоряющие химическую реакцию?
а) катализаторы
б) ингибиторы
5. Запишите уравнения химических реакций кислорода с азотом, калием, алюминием?
N2+O2↔2NO – Q,
2K+O2→K2O2,
4Al+3O2→2Al2O3
6. Самый распространенный химический элемент на Земле?
а) кислород
б) водород
в) кремний
Подводят итоги работы на уроке
Записывают дом. задание в дневник
задание в дневник
Опорные конспекты по химии (9 класс) – УчМет
МКОУ
Тополинская СОШ
ОПРОНЫЕ
КОНСПЕКТЫ
ПО
ХИМИИ
8
КЛАСС
Составитель
Сумцова
О.В.
Учитель
информатики-химии
2011г.
Электролитическая
диссоциация.
Процесс
распада электролита на ионы при
растворении его в воде или расплавлении
называют электролитической
диссоциацией.
Особенно осторожно
необходимо растворять серную кислоту,
так как из-за повышения температуры
часть воды может превратиться в пар и
под его давлением выбросить кислоту из
сосуда. Чтобы этого избежать,
серную
кислоту тонкой струей наливают в воду
(но не наоборот) при постоянном помешивании.
Растворение
– это физико-химический процесс.
Гидратация
– это присоединение воды к ионам, атомам
или молекулам. Продукты такого процесса
называют гидратами.
Кристаллические
вещества, в состав которых входит
связанная вода, называют кристаллогидратами.
Воду входящую в состав кристаллов,
называют кристаллизационной водой.
Основные
положения теории электролитической
диссоциации были сформулированы в 1887
году шведским ученым С.Аррениусом. в
настоящее время их можно сформулировать
следующим образом:
-
Электролиты
– это вещества, которые при растворении
в воде или в расплавленном состоянии
распадаются на ионы. Ионы – это атомы
или группы атомов, обладающие положительным
(катионы) или отрицательным (анионы)
зарядом. -
Ионы
отличаются от атомов как по строению,
так и по свойствам. -
В
растворе и расплаве электролита ионы
движутся хаотично. При пропускании
постоянного электрического тока через
этот раствор или расплав положительно
заряженные ионы (катионы) движутся к
катоду, а отрицательно заряженные иона
(анионы) – к аноду.
Диссоциация
кислот, оснований и солей.
Кислотой
называется вещество, которое при
взаимодействии с водой (при растворении
в воде) образует ионы оксония Н3О+
(или, упрощая, ионы водорода Н+)
СИЛЬНЫЕ:
HNO3, H2SO4, HI, HBr, HCl, H3PO4
СЛАБЫЕ:
H2SO3, CH3COOH, H2CO3,
H2S
МАЛОДИССОЦИИРУЮЩИЕ
ИЛИ ОЧЕНЬ
СЛАБЫЕ: H2SiO3
|
Формулы |
Специфический |
Образующиеся и |
|
H2SO4 |
Ион |
BaSO4 |
|
HCl |
Ион |
AgCl |
|
H2CO3 |
Известковая |
CaCO3 |
|
HNO3 |
Cu |
Выделение |
Химические
свойства кислот обеспечиваются ионами
водорода, в некоторых реакциях участвуют
анионы кислотных остатков( такие реакции
специфичны для каждой кислоты и называются
качественными).
Основания – это сложные
вещества, при диссоциации которых в
водных растворах в качестве анионов в
водных растворах в качестве анионов
отщепляются гидроксид-ионы.
Соли – это сложные вещества,
которые в водных растворах диссоциируют
на катионы металлов и анионы кислотных
остатков.
Кислые соли – это сложные
вещества, которые в водных растворах
диссоциируют на катионы металлов и
водорода и анионы кислотных остатков.
Алгоритм
составления
полных
и сокращенных ионных уравнений реакций.
1.
Напишите уравнение диссоциации
электронов, вступающих в реакцию
(обратите внимание на запись обозначения
зарядов ионов).
2.
Отметьте, при соединении каких ионов
могут образовываться малодиссоциирующие
соединения, и расставьте коэффициенты
(если нужно).
3.
Напишите формулу малодиссоциирующего
вещества и обозначения ионов, не
участвующих в реакции, в правой части
уравнения.
4.
Внимательно проверьте написанное! Сумма
положительно заряженных ионов в левой
и правой частях уравнения реакции должна
равняться нулю.
5.
Допишите знак равенства.
6.
Напишите сокращенное ионное уравнение
реакции, отражающее суть реакции ионного
обмена (образование малодиссоциирующих
веществ). Учтите, что вначале пишут
катион, а потом анион.
Окислительно-восстановительные
реакции
Реакции,
которые протекают с изменением степеней
окисления элементов, называют
окислительно-восстановительными.
При
составлением уравнений
окислительно-восстановительных реакций
пользуются следующим алгоритмом.
-
Пишем
формулы реагирующих веществ, ставим
стрелку, а за ней пишем формулы веществ,
которые образуются при данной реакции. -
Проставляем
степень окисления над знаками элементов,
у которых она меняется. -
Выписываем
химические знаки элементов, атомы или
ионы которых меняют степень окисления.
-
Находим,
сколько электронов отдают или принимают
соответствующие атомы или ионы. -
Находим
наименьшее общее кратное чисел отданных
и присоединенных электронов (их число
должно быть одинаково) -
Найденные
коэффициенты ставим перед соответствующими
формулами в правой части уравнения. -
Соответственно
найденным коэффициентам в правой части
уравнения находим коэффициенты для
формул всех остальных веществ. -
Проверяем,
соответствует ли число атомов всех
элементов в левой части уравнения числу
атомов в правой части уравнения.
С
водой не реагируют соли, образованные
сильным основанием и сильной кислотой,
так как ионы таких солей не могут
связываться с ионами Н+
и ОН—.
С
водой реагируют соли, образованные
или слабым основанием и сильной кислотой,
или сильным основанием и слабой кислотой.
Это объясняется тем, что в составе таких
солей имеются ионы, которые могут
связываться с ионами Н+
и ОН—.
Гидролиз
соли – это взаимодействие ионов
соли с водой с образованием малодиссоциирующих
электролитов.
Соли,
образованные слабой кислотой и слабым
основанием, в водном растворе не
существуют, потому что они или выпадают
в осадок, или разлагаются водой.
Гидролиз
соли – это обратимая реакция.
Гидролиз усиливается при нагревании и
сильном разбавлении раствора.
Кислород
и сера.
Явление,
когда один и тот же химический элемент
образует несколько простых веществ,
называют аллотропией. Простые
вещества, образованные одним и тем же
химическим элементом, называют аллотопными
видоизменениями этого элемента.
Химические
свойства серы.
|
Окислительные |
Восстановительные |
|
|
Сероводород.
Сероводород –
бесцветный газ, тяжелее воздуха, с
неприятным запахом тухлых яиц. Сероводород
очень ядовит. Уже 0,1% объема сероводорода
в воздухе вызывает тяжелые отравления.
Однако в малых количествах сероводород
полезен: при некоторых заболеваниях в
медицине используют сероводородные
ванны.
Сероводород
образуется при разложении без доступа
воздуха многих природных органических
веществ, содержится в вулканических
газах, в воде минеральных источников.
Все опыты с
сероводородом нужно проводить в вытяжном
шкафу!
Сероводород
легко можно получить в лаборатории
действием разбавленной серной кислоты
на сульфид железа (II):
FeS +H2SO4
= FeSO4
+ H2S↑
Эта
реакция проводится в аппарате Киппа,
который используют для получения
водорода.
Сероводород
горит на воздухе голубым пламенем, при
этом образуется сернистый газ, или оксид
серы (IV):
2H2S
+ 3O2
= 2H2O
+2SO2
При
недостатке кислорода образуются пары
воды и сера:
2H2S
+ O2 =
2H2O
+2S
Сероводород
обладает свойствами восстановителя.
Если в пробирку с небольшим количеством
сероводородной воды прилить бромную
воду, то раствор обесцвечивается. На
поверхности раствора появляется сера:
H2S
+ Br2
= 2HBr +S
Сероводород
малорастворим в воде. При 20° в одном
При 20° в одном
объеме воды растворяется 2,4 объема
сероводорода. Водный раствор сероводорода
проявляет свойства слабой кислоты:
H2S
↔HS—
+ H+
HS—↔
S2- +
H+
Сероводородная
кислота вступает со щелочами в реакцию
нейтрализации:
H2S + NaOH = NaHS +
H2O
избыток
H2S + 2NaOH = Na2S
+ 2H2O
избыток
Средние
соли сероводородной кислоты называют
сульфидами, а кислые – гидросульфидами.
В воде
растворимы сульфиды щелочных
металлов и большинство гидросульфидов.
Сернистый
газ. Сернистая кислота.
При
горении серы на воздухе образуется
сернистый газ, или оксид серы (IV)
SO2.
Это бесцветный газ с резким характерным
запахом, более чем в 2 раза тяжелее
воздуха, хорошо растворяется в воде,
ядовит.
SO2кислотный оксид.
H2O
+ SO2
↔ H2SO3
реакция обратимая.
Сернистая
кислота – неустойчивое соединение,
легко распадается на оксид серы (IV)
и воду. Эта кислота средней силы. Она
образует два ряда солей: средние –
сульфиты и кислые гидросульфиты.
Качественной
реакцией на сульфиты является
взаимодействие соли с сильной кислотой,
при этом выделяется газ SO2
с резким запахом.
Сернистый
газ как кислотный оксид взаимодействует
с щелочами и основными оксидами.
Серная
кислота (разбавленная)
Химическая
формула H2SO4
Структурная
формула
О
│
HO
– S – OH
│
О
Уравнение
диссоциации
H2SO4
= 2H+
+ SO42-
сильный электролит
Правила
техники безопасности при приготовлении
раствора серной кислоты
Кислоту
нужно небольшими порциями вливать в
воду.
Химические
свойства
Me
(в ряду активности до Н2)
MeSO4
+ H2↑
MeO
MeSO4
+ H2O
MeOH
H2SO4
+
MeSO4 + H2O
(разб.)
MeR (в случае ↑
или ↓)
MeSO4
+ HR
BaR
(качественная реакция)
Белый
осадок BaSO4↓
+ HR
Производство
серной кислоты:
FeS2
→ SO2
→ SO3 →
H2SO4
Скорость
химических реакций. Химическое равновесие.
Химическое равновесие.
Скорость
химической реакции определяется
изменением концентрации одного из
реагирующих веществ в единицу времени.
Условия,
влияющие на скорость химических реакций.
-
Скорость
химических реакций зависит от природы
реагирующих веществ. -
Для
веществ в растворенном состоянии и
газов скорость химических реакций
зависит от концентрации реагирующих
веществ. -
Для
веществ в твердом состоянии скорость
реакции прямо пропорциональна поверхности
реагирующих веществ. -
При
повышении температуры на каждые 10°С
скорость большинства реакций увеличивается
в 2-4 раза. -
Скорость
химических реакций зависит от присутствия
некоторых веществ. (катализаторов,
ингибиторов).
Вещества,
которые ускоряют химические реакции,
но сами при этом не расходуются, называют
катализаторами.
Вещества,
которые замедляют скорость химических
реакций, называют ингибиторами.
Химические
реакции, которые протекают одновременно
в двух противоположных направлениях –
прямом и обратном, — называю обратимыми
реакциями.
Состояние
системы, при котором скорость прямой
реакции равна скорости обратной реакции,
называют химическим равновесием.
Принцип
Ле Шателье: при изменении внешних
условий химическое равновесие смещается
в сторону той реакции (прямой или
обратной), которая ослабляет это внешнее
воздействие.
При
повышении температуры равновесие
смещается в сторону эндотермического
процесса.
При
повышении давления равновесие
смещается в сторону меньшего объема.
При
увеличении концентрации одного из
исходных веществ равновесие
смещается в сторону образования новых
веществ.
При
увеличении концентрации продукта
реакции равновесие смещается в
сторону исходных вещества.
Катализаторы
не влияют на смещение химического
равновесия, они способствуют более
быстрому достижению равновесия.
Азот.
Молекула
азота – N2,
структурная формула N Ξ
N, электронная формула
:N: :N:
В
молекуле азота одна σ-связь и две π-связи.
Азот
находится в воздухе в свободном виде –
78% по объему.
Физические
свойства. Азот – газ без цвета и
запаха, немного легче воздуха. Растворимость
его в воде незначительна. Азот в твердом
состоянии имеет молекулярную
кристаллическую решетку, поэтому у него
низкие температуры плавления и кипения.
Химические
свойства. При обычных условиях азот
малоактивен
Аммиак.
Молекулярная
формула – NH3
Физические
свойства – бесцветный газ с характерным
резким запахом, почти в два раза легче
воздуха, очень хорошо растворим в воде.
При повышении давления аммиак сжижается.
Жидкий аммиак имеет большую теплоту
испарения, поэтому его применяют в
холодильных устройствах.
Химические
свойства.
-
При
нагревании разлагается:
2NH3 ↔ N2
+ 3H2
-
Горит
в кислороде:
4NH3 + 3O2
→ 2N2 + 6H2O
-
В
присутствии катализатора (сплав платины
и родия) окисляется кислородом воздуха
4NH3 + 5O2
→ 4NO + 6H2O
-
Реагирует
с водой
NH3 + H2O→ NH4+ + OH—
-
Реагирует
с кислотами, образуя нормальные и кислые
соли
NH3
+ HCl →
NH4Cl
NH3
+ H2SO4
→ NH4HSO4
2NH3
+ H2SO4
→ (NH4)2SO4
Соли аммония.
Физические
свойства. Все соли аммония – твердые
кристаллические вещества, хорошо
растворимы в воде.
Химические
свойства.
-
Сильные
электролиты, диссоциируют на ионы
NH4R →
NH4+ + R
-
Реагируют
с кислотами
NH4R + HR1
→ NH4R1+ HR
-
Реагируют
с другими солями
NH4R + MeR1
→ NH4R1 + MeR
-
Подвергаются
гидролизу -
При
комнатной температуре разлагаются
NH4R →
NH3↑ + HR
-
Реагируют
со щелочами
NH4R
+ MeOH → MeR +
NH3↑
+ H2O
Оксиды
азота.
|
Признаки |
N2O |
NO |
NO2 |
N2O3 |
N2O5 |
|
Агрегатное |
Газ |
Жидкость |
Твердое |
||
|
Цвет |
Бесцветный |
Бурый |
Темно |
Белое |
|
|
Токсичность |
— |
+ |
|||
|
Отношение |
Малорастворим |
Химически |
|||
|
Кислотно-основные |
Восстановительные |
Окисли-тельно |
Окислительные |
||
|
Особые |
Разлагается |
Окисляется |
+ |
Разлагается |
|
|
Получение |
Из |
Окислением |
Из |
Из |
Обезво-живани-ем |
|
Применение |
Медицина |
Замедление |
Производство HNO3 |
Промышленного |
|
Азотная
кислота.
Физические
свойства. Чистая азотная кислота –
бесцветная дымящаяся жидкость с резким,
раздражающим запахом. Концентрированная
азотная кислота обычно окрашена в желтый
цвет.
Химические
свойства.
Me
MeNO3
+ (различные оксиды азота, азот, аммиак)
MeO
MeNO3
+ H2O
MeOH
HNO3
+
MeNO3 + H2O
(разб.)
MeR (более слабых
кислот)
MeNO3
+ HR
Белок
(качественная реакция)
Вещество
ярко-желтого цвета.
Cu
+ 4HNO3 → Cu(NO3)2 + 2NO2↑
+ 2H2O
Cu0
– 2e— → Cu+2 1
N+5
+ e— → N+4 2
3Cu
+ 8HNO3 → 3Cu(NO3)2 + 2NO↑ +
4H2O
Cu0
– 2e— → Cu+2 3
N+5
+3e— → N+4 2
Производство
азотной кислоты: NH3
→ NO→ NO2
→ HNO3
Соли
азотной кислоты.
Соли
азотной кислоты называют нитратами.
Нитраты
образуются при взаимодействии: 1) металлов
основных оксидов, оснований, аммиака и
некоторых солей с азотной кислотой; 2)
оксида азота (IV) со щелочами.
Физические
свойства. Все нитраты – твердые
кристаллические вещества, хорошо
растворимые в воде.
Химические
свойства.
Me
находится левее Mg MeNO2
+ O2↑
MeNO3
t Me находится между
Mg и Cu MeO + NO2↑ + O2↑
Me
находится правее Cu Me
+ NO2↑
+ O2↑
t
NH4NO3
→ N2O↑ + 2H2O
Для
качественного определения нитрат ионов
в пробирку помещают исследуемое вещество,
добавляют медных стружек, приливают
концентрированную азотную кислоту и
нагревают. Выделение газообразного
Выделение газообразного
оксида азота (IV) бурого
цвета свидетельствует о наличии
нитрат-ионов NO3—.
Фосфор.
В
свободном состоянии фосфор образует
несколько аллотропных видоизменений:
красный, белый и черный фосфор. а –
молекулы белого фосфора, б – кристаллическая
решетка черного фосфора, в – кристаллическая
решетка красного фосфора.
Из-за
большой активности фосфор в природе
встречается только в соединениях.
Фосфор
получают из фосфоритов и апатитов,
нагревая их в электрической печи без
доступа воздуха в присутствии оксида
кремния (IV) и угля.
Физические
свойства.
Белый
фосфор. Кристаллическое вещество,
можно резать ножом (под водой). Бесцветный
с желтоватым оттенком. Имеет чесночный
запах. Плотность 1,8г/см3. В воде не
растворяется. Хорошо растворяется в
сероуглероде. Температура плавления.
44°С. Температура воспламенения 40°С. В
В
измельченном состоянии воспламеняется
при обычной температуре. В темноте
светится. Сильный яд.
Красный
фосфор. Аморфное или кристаллическое
вещество. Темно-красного цвета. Без
запаха. Плотность 2,3г/см3. В воде
и сероводороде не растворяется. При
сильном нагревании превращается в пары
белого фосфора. Температура воспламенения
примерно 260°С. Не светится, не ядовит.
Химические
свойства.
O2
→ P2O5
Р
+ H2 → PH3
Me → MeP
Оксид
фосфора (V).
Физические
свойства. Оксид фосфора
(V) = белый рыхлый порошок,
чрезвычайно гигроскопичный. Поэтому
его следует хранить в герметически
закрытых сосудах.
Химические
свойства. По химическим свойствам
сходен с другими кислотными оксидами.
t
P2O5
+ H2O → 2HPO3
P2O5 + H2O → 2H3PO4
Ортофосфорная
кислота и ее соли.
Физические
свойства. Твердое кристаллическое
вещество, бесцветное, хорошо растворимое
в воде.
Химические
свойства.
Водный
раствор кислоты изменяет окраску
индикатора. Диссоциация происходит
ступенчато.
H3PO4
↔ H+
+ H2PO4—
H2PO4
↔ H+
+ HPO4—
HPO4
↔ H+
+ PO4—
Me
MeРO4
+ Н2↑
MeO
MeРO4
+ H2O
MeOH
H3PO4
+
MeРO4
+ H2O
MeR
(более слабых
кислот)
MeРO4
+ HR
AgNO3
(качественная реакция)
Желтый
осадок.
При
нагревании постепенно превращается в
метафосфорную кислоту.
2H3PO4
→ H4P2O7
(дифосфорная кислота) + H2O
H4P2O7
→ 2HPO3
(метафосфорная кислота) + H2O
Ортофосфорная
кислота играет большую роль в
жизнедеятельности животных и растений.
Ее остатки входят в состав аденозинтрифосфорной
кислоты АТФ.
При
разложении АТФ выделяется большое
количество энергии.
Ортофосфаты.
Ортофосфорная
кислота образует три ряда солей.
MeРO4
– ортофосфаты
MeНРO4
– гидроортофосфаиы
Me
Н2РO4
– дигидроортофосфаты
Вместо
иона одновпалентного металла в состав
ортофосфатов может входить ион аммония:
(NH4)3PO4
— ортофосфат аммония,
(NH4)2
HPO4
— гидроортофосфат аммония,
NH4H2PO4
— дигидроортофосфат аммония.
Ортофосфаты
и гидроортофосфаты кальция и аммония
широко используются в качестве удобрений,
ортофосфат и гидроортофосфат натрия –
для осаждения из воды солей кальция.
ГДЗ конспекты по физике 9 класс ответы и решения онлайн
Умение составлять краткую запись урока, темы — один из важнейших навыков, которым должен овладеть выпускник. Особенно важно конспектирование по сложным дисциплинам, например, таким как физика. Этот предмет наиболее ярко показывает необходимость постоянного использования теоретических знаний на практике. Но чем глубже, точнее понята теория, тем лучше умение ее практического применения. Именно поэтому конспекты по физике за 9 класс — важная часть урока по этому предмету, одно из базовых заданий, которое дают выполнять педагоги, которому учат в школе. Нередко задача законспектировать параграф или дополнительный материал предлагается к самостоятельному выполнению, например, в качестве домашней работы с последующей проверкой результата учителем.
С какими трудностями сталкиваются учащиеся при ведении конспектов?
Зачастую конспекты по физике в 9 классе представляют сложность для школьников-девятиклассников. Это связано с тем, что ранее, в средней и старшей школе, ими не были сформированы навыки:
- быстрого чтения и обдумывания, логической обработки больших объемов материала;
- выделения главной мысли или ее самостоятельной формулировки на основе прочитанной информации;
- систематизации данных, составления и записывания выводов, предложенных в учебных пособиях или сделанных самостоятельно в сжатом, удобном для последующего использования в работе, виде.
Научиться конспектировать информацию по этой дисциплине необходимо. Это позволит впоследствии:
- быстро запоминать большие блоки данных, даже по самой сложной тематике, разделу;
- находить и срочно применять ту или иную информацию — закон, формулу, выводы по проведенному опыту, эксперименту и т. п.
 ;
; - успешно готовиться к зачету, экзамену, опросу по дисциплине, поскольку грамотно составленная краткая запись наглядна и удобна в использовании, в том числе — в условиях ограниченного времени на выполнение заданий.
Где набраться знаний в области грамотной записи уроков?
Умению составлять конспекты по физике за 9 класс можно научиться, для этого необязательно прибегать к сторонней помощи, например, репетиторской. Обширная коллекция конспектов по этой дисциплине для девятиклассников содержится на портале Еуроки. Воспользовавшись платформой, каждый выпускник сможет:
- найти нужный для себя материал и применить его;
- просмотреть, оценить и запомнить, как следует грамотно записать тему, раздел в сжатом, удобном для последующего применения, виде;
- в целом научиться конспектировать, понять логику и методику составления таких записей.
Площадка будет полезна не только для самих школьников. Её успешно применяют и педагоги-предметники, составляя план, программу своих уроков. И репетиторы, руководители предметных кружков, курсов для подачи большого объема информации в доступной, сжатой форме. И родители, которые желают проверить знания своего ребенка, но не хотят вникать в программу, курс дисциплины.
И репетиторы, руководители предметных кружков, курсов для подачи большого объема информации в доступной, сжатой форме. И родители, которые желают проверить знания своего ребенка, но не хотят вникать в программу, курс дисциплины.
Конспект урока на тему «кальций и его соединения» 9 класс | Уроки по Химии
Конспект урока на тему «кальций и его соединения» 9 класс
15.02.2017
1757
414
Савинская Татьяна Андреевна
Урок № 34. ХИМИЯ 9 класс Дата_______________
Тема урока: Кальций и его соединения. Важнейшие месторождения соединений кальция в Казахстане. Демонстрации №3 (3.1,3.2) образцы природных соединений кальция
Цель урока: учащиеся знают положение кальция в периодической системе, свойства, кальция. Умеют записывать уравнения реакций, характеризующие свойства его соединений.
Ожидаемые результаты: учащиеся дают характеристику кальцию по положению в ПС и строению атома, записывают уравнения химических реакций, характерные для кальция, оксида и гидроксида. Называют применение основных соединений кальция.
Называют применение основных соединений кальция.
Тип урока: изучения нового материала
Формы работы учащихся: групповая, индивидуальная
Оборудование: учебная презентация, образцы природных соединений кальция
Ход урока
Этапы Деятельность учителя Деятельность учащихся
1.организа
ционный Приветствие, настрой. Приветствие, готовность к уроку, деление на группы ( глюконат кальция с номерами на упаковке)
3. Стадия вызова
определение темы и целеполагание Сложите вместе ваши номера на упаковке, в которой находятся таблетки, прочтите названия и определите тему урока.
Какова цель урока? В каких случаях прописывают клюконат кальция? Каков его состав?
Отвечают
Определяют тему, формулируют цель урока.
Рассуждают, высказывают предположения.
3.Стадия осмысления
Метод «Автобусная остановка» 1 группа: кальций
2.группа: оксид кальция
3 группа: гидроксид кальция
4 группа: “Важнейшие соединения кальция, получаемые в промышленности”. Природные соединения кальция
Природные соединения кальция
Предлагает взаимообмен информацией.
Взаимооценивание на стикерах.
1 группа: характеризуют кальций
2 группа: оксид кальция
3 группа- гидроксид кальция
4 группа заполняют таблицу “Важнейшие соединения кальция, получаемые в промышленности”. Природные соединения кальция рассматривают и оставляют для других групп.
Название соединения Формула Применение
Переходим к следующему автобусу, в течение 5 мин знакомятся с информацией, записывают в тетрадь кратко нужную информацию.
Проводят взаимооценивание по составленным критериям
Итог Показ презентации о важнейших месторождениях соединений кальция в РК, ролик взаимодействия кальция с водой Делают вывод о распространенности с кальция в природе, ( 5 место)его химической активности
рефлексия Предлагает задание: мини-тест
Самопроверка, критерии проговаривает учитель
Мнение учащихся об уроке.
«Рефлексивная мишень» Выполняют тест.
Секторы: было интересно, активно участвовал, было понятно, узнал новое
Домашнее задание Задает параграфы учебника, составить по 2 вопроса, составить тест по теме из 10 вопросов на выбор Записывают Д/З
Полный текст материала смотрите в скачиваемом файле.

На странице приведен только фрагмент материала.
Сера — урок. Химия, 8–9 класс.
Химический элемент
Сера — химический элемент № \(16\). Она расположена в VIА группе третьем периоде Периодической системы.
S16+16)2e)8e)6e
На внешнем слое атома серы содержатся шесть валентных электронов. До завершения внешнего слоя не хватает двух электронов. Поэтому в соединениях с металлами и водородом сера проявляет степень окисления \(–2\). При взаимодействии с более электроотрицательными элементами (кислородом, галогенами) сера образует соединения, в которых её степень окисления положительная (\(+4\) или \(+6\)).
В земной коре сера встречается в самородном виде или в виде минералов и горных пород: (пирит — FeS2, цинковая обманка — ZnS, свинцовый блеск — PbS, гипс — CaSO4⋅2h3O, глауберова соль — Na2SO4⋅10h3O).
|
Рис. |
Рис. \(2\). Пирит |
Сера относится к макроэлементам живых организмов. Она содержится в белках. Больше всего серы в белках, которые образуют шерсть, волосы, рога. Входит она также в состав некоторых витаминов и гормонов.
Простое вещество
Сера образует несколько аллотропных модификаций. Обычно мы имеем дело с кристаллической серой, которая состоит из восьмиатомных циклических молекул.
Рис. \(3\). Модель молекулы серы
Молекулы образуют кристаллы разного строения, и поэтому существуют аллотропные видоизменения: ромбическая и моноклинная сера. Обе модификации представляют собой жёлтые легкоплавкие вещества. Температуры плавления их несколько различаются (\(+112,8\) °С и \(+119,3\) °С).
Рис. \(4\). Сера
При нагревании сера плавится, превращается в лёгкую жидкость, а затем начинает темнеть и становится вязкой. Образуется пластическая сера, состоящая из длинных линейных молекул.
Образуется пластическая сера, состоящая из длинных линейных молекул.
В воде сера не растворяется и ею не смачивается. Поэтому порошок серы не тонет в воде, несмотря на более высокую плотность (\(2,07\) г/см³). Такое явление называется флотацией.
Подожжённая сера реагирует с кислородом, и образуется сернистый газ. Сера в этой реакции — восстановитель.
S0+O20=tS+4O2−2.
Окислительные свойства сера проявляет в реакциях с металлами и водородом.
С активными металлами и ртутью реагирует при комнатной температуре:
Hg0+S0=Hg+2S−2.
При нагревании сера вступает в реакцию с большинством металлов — железом, алюминием, цинком и другими, кроме золота и платины.
2Al0+3S0=tAl+32S−23.
В реакциях с металлами образуются сульфиды.
При повышенной температуре сера реагирует с водородом. Образуется сероводород:
h30+S0=th3+1S−2.
Применение серы
- Используется в химической промышленности для производства серной кислоты;
- находит применение в сельском хозяйстве для обеззараживания помещений;
- входит в состав некоторых мазей;
- используется в производстве спичек и бумаги;
- с её помощью каучук превращают в резину;
- входит в состав взрывчатых веществ.
Источники:
Рис. 1. Самородная сера https://image.shutterstock.com/image-photo/raw-sulphur-sulfur-ore-cutout-600w-1646293537.jpg
Рис. 2. Пирит https://www.shutterstock.com/ru/image-photo/pyrite-mineral-sulfide-group-1734246830
Рис. 3. Модель молекулы серы © ЯКласс
Рис. 4. Сера https://upload. wikimedia.org/wikipedia/commons/thumb/4/44/Sulfur-sample.jpg/1280px-Sulfur-sample.jpg
wikimedia.org/wikipedia/commons/thumb/4/44/Sulfur-sample.jpg/1280px-Sulfur-sample.jpg
Не могу конспекты составить Химия, 8 класс, параграф 32, 9 вопрос. Рудзитис и Фельдман
Оо, столько времени вообще ушло на него((
Соляная кислота HCl
Общая характеристика. Сильная одноосновная кислота.
Нахождение в природе. Входит в состав желудочного сока. На одном из Курильских островов есть озеро, заполненное концентрированным раствором серной и соляной кислот.
Получение.
а) в лаборатории:
Н2 + Сl2 → 2 НСl
H2SO4(конц) + 2 NaCl → Na2SO4 + 2 HCl ↑
(этим способом соляную кислоту получают и в промышленности)
б) в промышленности:
Физические свойства. Бесцветная, «дымящая» на воздухе, едкая жидкость. Плотность раствора 1,19 г/см3. Молярная масса 36,46 г/моль. При затвердевании даёт кристаллогидраты составов НСl · Н2O, НСl · 2 Н2O, НСl · 3H2O, НСl · 6Н2O. Хлороводород растворим в воде. При попадании на кожу вызывает ожоги.
Хлороводород растворим в воде. При попадании на кожу вызывает ожоги.
Химические свойства.
2Na + 2HCl → 2NaCl + H2
Al2O3 +6 HCl → 2 AlCl3 + 3 H2O
Mg(OH)2 + 2 HCl → MgCl2 + 2 H2O
Na2CO3 + 2 HCl → 2 NaCl + H2O + CO2
2 KMnO4 + 16 HCl → 5Cl2 + 2 MnCl2 + 2 KCl + 8H2O
NH3 + HCl → NH4Cl
Применение. В промышленности для очистки поверхности металлов, для получения хлоридов, в пищевой промышленности в качестве БАД, в медицине для нормализации кислотности желудочного сока.
Серная кислота H2SO4
Общая характеристика. Сильная двухосновная кислота, содержащая атом серы в высшей степени окисления.
Нахождение в природе. В некоторых водах вулканического происхождения. В атмосфере Венеры и некоторых других небесных тел.
Получение.
а) в лаборатории:
CuSO4 + H2S → CuS + H2SO4
H2SO3 + H2O2 → H2SO4 + H2O
б) В промышленности сначала получают SO3, а затем проводят реакцию:
Н2O + SO3 → H2SO4·
Реакция проходит с выделением тепла, поэтому H2SO4 смешивают с SO3.
Так же получают серную кислоту из железного купороса:
2 FeSO4 · 7 Н2O → Fe2O3 + SO2 + Н2O + O2
SO2 + Н2O + O2 <—> H2SO4
Физические свойства. При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета и запаха. Смешивается с водой и S03 во всех соотношениях.
В водных растворах серная кислота практически полностью диссоциирует на Н+, HSO4-, и SO2-. Образует гидраты H2SO4 · nН2O, где п = 1, 2, 3, 4, 5, 6.
Образует гидраты H2SO4 · nН2O, где п = 1, 2, 3, 4, 5, 6.
Химические свойства.
Серная кислота — сильный окислитель.
8 Na + 5 H2SO4(конц) → H2S + 8 Н2O + 4 Na2SO4
Сu + H2SO4(кohhнц) → SO2 + CuSO4 + 2 H2O
Zn + H2SO4(paзб) → ZnSO4 + H2O
S + 2 H2SO4(конц) → 3 S + 4 O2 + 2 H2O
2 P+5 H2SO4(koнц) → 5 S+4 O2+2 H3PO4+2 H2O
CuO + H2SO4 → CuSO4 + H2O
H2SO4 + 2 NaOH → Na2SO4 + 2 H2O
BaCl2 + H2SO4 → BaSO4 + 2 HCl
Применение. Серную кислоту применяют в производстве минеральных удобрений, как электролит в свинцовых аккумуляторах, в химической промышленности для получения кислот и солей, в пищевой промышленности в качестве эмульгатора, в органическом синтезе.
Ортофосфорная кислота Н3РO4
Общая характеристика. Трехосновная кислота средней силы.
Нахождение в природе. В природе встречаются ортофосфаты — соли фосфорной кислоты в виде минералов — вивианит (Fe2+, Fe3+) [ΡО4]·8Η2O, торбернит Cu(UO2)2[PO4]2 · 12Н2O, отенит Ca(UO2)2[PO4]2 ∙ 8Н2O, бирюза СuАl6[РO4]4(OН)8 · 4Н2O и другие.
Получение:
а) в лаборатории:
Р2O5 + 3 Н2O → 2 Н3РO4
Са3(РO4)2 + 3 H9SO4 → 3 CaSO4 + 2 Н3РO4
РСl5 + 4 Н2O → Н3РO4 + 5 НСl
3 Р + 5 ΗΝO3 + 2 Н2O → 3 Н3РO4 + 5 NO
б) В промышленности получают сначала Р4О10, затем производят гидратацию:
Р4О10 + 6Н2О→4Н3РO4
Физические свойства. При нормальных условиях представляет собой бесцветные гигроскопичные кристаллы. При температуре выше 213 ° С она превращается в пирофосфорную кислоту Н4Р2O7. Хорошо растворима в воде и этаноле.
При нормальных условиях представляет собой бесцветные гигроскопичные кристаллы. При температуре выше 213 ° С она превращается в пирофосфорную кислоту Н4Р2O7. Хорошо растворима в воде и этаноле.
Химические свойства.
Н3РO4 + 3 AgNO3 Ag3PO4 ↓
(желтый) + 3 ΗΝO3
6 Na + 2 Н3РO4 → 2 Na3PO4 + 3 H2 ↑
3 CaO + 2 H3PO4 → Ca3(PO4)2 + 3 H2O
H3PO4 + 3 NaOH → Na3PO4 + 3 H2O
H3PO4 + 2 NaOH → Na2HPO4 + 2 H2O
H3PO4 + NaOH → NaH2PO4 + H2O
Применение. Применяется при пайке по черному металлу или нержавеющей стали, в составе фреонов в промышленных морозильных установках, для очищения поверхностей от ржавчины и для предотвращения коррозии металлов.
конспект уроку для учнів 9 класу
Конспект уроку для учнів 9 класу з використанням QR-кодів, взято до уваги підручник « О.В. Григорович ; Хімія 9 клас ; «Ранок» 2017р»
Тема уроку: Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки.
Мета уроку: Ознайомити учнів з поняттям ступінь окиснення, з основними правилами визначення ступенів окиснення. Формувати вміння визначати ступені окиснення елемента за хімічною формулою сполуки. Розвивати інтерес до предмета, інформаційно-комунікативну, здоров’язбережувальну компетентності, вміння працювати у групах. Виховувати дружелюбність, самостійність, наполегливість, відповідальність.
Тип уроку: вивчення нового матеріалу
Обладнання та реактиви: Періодична система хімічних елементів Д.І. Менделєєва,картки з QR-кодами, мобільні пристрої для зчитування QR-кодів, картки з індивідуальними завданнями.
Хронометраж уроку:
І. Організаційний момент 1- 2хв
ІІ. Актуалізація теоретичних знань. 5-6хв.
ІІІ. Мотивація навчально-пізнавальної діяльності 2-3хв.
ІV. Вивчення нового матеріалу 16-18хв.
V. Узагальнення та систематизація знань 10-12хв.
VІ. Підсумки уроку та виставлення оцінок 3-4 хв.
VІІ. Інструктаж з Д/З 1-2хв.
Хід уроку:
І. Організаційний момент
Перевірка присутніх, вияснення організаційних питань.
ІІ.Актуалізація теоретичних знань.
Двоє учнів працюють біля дошки зі схемами
Хімічні елементи ―›› Речовини
↙ ↘ ↙ ↘
Фронтальне опитування:
— Які речовини називають простими?
— де в Періодичній системі хімічних елементів Д.І. Менделєєва розміщені металічні елементи?
— який з неметалічних елементів має найбільшу електронегативність?
ІІІ.Мотивація навчально-пізнавальної діяльності
Напис на дошці :« У мене немає ніякого таланту,є лише наполегливість та допитливість» А.Енштейн.
Запитання:
-Хто такий А.Енштейн?
-Як ви розумієте цей вислів?
Я бажаю вам бути допитливими, наполегливими, відповідальними як на сьогоднішньому уроці так і на протязі всього життя. На сьогоднішньому уроці ви матимете можливість дізнатися багато нового та цікавого і вам неодмінно знадобляться ці якості.
На сьогоднішньому уроці ви матимете можливість дізнатися багато нового та цікавого і вам неодмінно знадобляться ці якості.
ІV.Вивчення нового матеріалу
—Робота учнів з підручником. Учні ознайомлюються з поняттям « ступінь окиснення»
-Розповідь вчителя з елементами бесіди: ступінь окиснення позначать використовуючи знаки «+», «-» або «0». Наприклад: H₂⁺¹S⁺⁶ O4¯²
Постановка проблемного питання— «у сполуці повинно бути більше «+» чи «-»?.
Діти висловлюють власні думки. Вчитель вказує на те, що «+» і «-» має бути порівну і у сумі давати«0», адже молекула — електронейтральна.
А як же визначити ,який саме ступінь окиснення матиме хімічний елемент у тій чи іншій сполуці ?
Для цього існують певні правила, з якими ви зможете ознайомитися відкривши QR-коди за допомогою власних мобільних приладів.
— Робота в групах. Кожна група отримує комплект QR-кодів, за кожним з яких зашифровано по 1 правилу визначення ступенів окиснення та приведено приклади. Учні відкривають по одному правилу, записують їх та опрацьовують приклади.
Учні відкривають по одному правилу, записують їх та опрацьовують приклади.
— Оздоровча рухова вправа
V. Узагальнення та систематизація знань .
І. Групи отримують нові QR-коди, розкривши які, отримують завдання на визначення ступенів окиснення хімічних елементів у сполуках.
2. Визначте ступені окиснення елементів, речовин, які беруть участь у процесах : фотосинтезу, горіння сірки. Напишіть відповідні рівняння реакцій.
VІ. Підсумки уроку та виставлення оцінок
Рефлексія:
- Що нового ви дізналися на сьогоднішньому уроці?
- Що вам сподобалося найбільше?
- Що не сподобалося?
Виставлення оцінок
VІІ.Інструктаж з Д/З
Опрацювати параграф підручника, завд № 1-3, №6*
Додатковий матеріал до уроку
QR-коди:
открытых учебников | Сиявула
Математика
Наука
-
- Читать онлайн
-
Учебники
-
Английский
-
Класс 7А
-
Класс 7Б
-
Класс 7 (объединенные А и В)
-
-
Африкаанс
-
Граад 7А
-
Граад 7Б
-
Graad 7 (A en B saam)
-
-
-
Пособия для учителя
-
- Читать онлайн
-
Учебники
-
Английский
-
Класс 8А
-
Класс 8Б
-
Класс 8 (объединенные А и В)
-
-
Африкаанс
-
Граад 8А
-
Граад 8Б
-
Graad 8 (A en B saam)
-
-
-
Пособия для учителя
-
- Читать онлайн
-
Учебники
-
Английский
-
Класс 9А
-
Класс 9Б
-
Класс 9 (объединенные А и В)
-
-
Африкаанс
-
Граад 9А
-
Граад 9Б
-
Graad 9 (A en B saam)
-
-
-
Пособия для учителя
-
- Читать онлайн
-
Учебники
-
Английский
-
Класс 4А
-
Класс 4Б
-
Класс 4 (объединенные A и B)
-
-
Африкаанс
-
Граад 4А
-
Граад 4Б
-
Graad 4 (A en B saam)
-
-
-
Пособия для учителя
-
- Читать онлайн
-
Учебники
-
Английский
-
Класс 5А
-
Класс 5Б
-
Класс 5 (объединенные A и B)
-
-
Африкаанс
-
Граад 5А
-
Граад 5Б
-
Graad 5 (A en B saam)
-
-
-
Пособия для учителя
-
- Читать онлайн
-
Учебники
-
Английский
-
Класс 6А
-
Класс 6Б
-
Класс 6 (объединенные A и B)
-
-
Африкаанс
-
Граад 6А
-
Граад 6Б
-
Graad 6 (A en B saam)
-
-
-
Пособия для учителя
Лицензирование нашей книги
Эти книги не только бесплатны, но и имеют открытую лицензию! Один и тот же контент, но разные версии (фирменные или нет) имеют разные лицензии, как объяснено:
CC-BY-ND (фирменные версии)
Вам разрешается и поощряется свободное копирование этих версий. Вы можете копировать, распечатывать и распространять их столько раз, сколько захотите. Вы можете загрузить их на свой мобильный телефон, iPad, ПК или флешку. Вы можете записать их на компакт-диск, отправить по электронной почте или загрузить на свой веб-сайт. Единственное ограничение заключается в том, что вы не можете каким-либо образом адаптировать или изменять эти версии учебников, их содержание или обложки, поскольку они содержат соответствующие бренды Siyavula, логотипы спонсоров и одобрены Департаментом базового образования. Для получения дополнительной информации посетите Creative Commons Attribution-NoDerivs 3.0 Непортированный.
Вы можете копировать, распечатывать и распространять их столько раз, сколько захотите. Вы можете загрузить их на свой мобильный телефон, iPad, ПК или флешку. Вы можете записать их на компакт-диск, отправить по электронной почте или загрузить на свой веб-сайт. Единственное ограничение заключается в том, что вы не можете каким-либо образом адаптировать или изменять эти версии учебников, их содержание или обложки, поскольку они содержат соответствующие бренды Siyavula, логотипы спонсоров и одобрены Департаментом базового образования. Для получения дополнительной информации посетите Creative Commons Attribution-NoDerivs 3.0 Непортированный.
Узнайте здесь больше о спонсорстве и партнерстве с другими, которые сделали возможным выпуск каждого из открытых учебников.
CC-BY (версии без торговой марки)
Эти небрендированные версии одного и того же контента доступны для совместного использования, адаптации, преобразования, изменения или дальнейшего развития любым способом, при единственном требовании — отдать должное Сиявуле. Для получения дополнительной информации посетите Creative Commons Attribution 3.0 Unported.
Для получения дополнительной информации посетите Creative Commons Attribution 3.0 Unported.
открытых учебников | Сиявула
Математика
Наука
-
- Читать онлайн
-
Учебники
-
Английский
-
Класс 7А
-
Класс 7Б
-
Класс 7 (объединенные А и В)
-
-
Африкаанс
-
Граад 7А
-
Граад 7Б
-
Graad 7 (A en B saam)
-
-
-
Пособия для учителя
-
- Читать онлайн
-
Учебники
-
Английский
-
Класс 8А
-
Класс 8Б
-
Класс 8 (объединенные А и В)
-
-
Африкаанс
-
Граад 8А
-
Граад 8Б
-
Graad 8 (A en B saam)
-
-
-
Пособия для учителя
-
- Читать онлайн
-
Учебники
-
Английский
-
Класс 9А
-
Класс 9Б
-
Класс 9 (объединенные А и В)
-
-
Африкаанс
-
Граад 9А
-
Граад 9Б
-
Graad 9 (A en B saam)
-
-
-
Пособия для учителя
-
- Читать онлайн
-
Учебники
-
Английский
-
Класс 4А
-
Класс 4Б
-
Класс 4 (объединенные A и B)
-
-
Африкаанс
-
Граад 4А
-
Граад 4Б
-
Graad 4 (A en B saam)
-
-
-
Пособия для учителя
-
- Читать онлайн
-
Учебники
-
Английский
-
Класс 5А
-
Класс 5Б
-
Класс 5 (объединенные A и B)
-
-
Африкаанс
-
Граад 5А
-
Граад 5Б
-
Graad 5 (A en B saam)
-
-
-
Пособия для учителя
-
- Читать онлайн
-
Учебники
-
Английский
-
Класс 6А
-
Класс 6Б
-
Класс 6 (объединенные A и B)
-
-
Африкаанс
-
Граад 6А
-
Граад 6Б
-
Graad 6 (A en B saam)
-
-
-
Пособия для учителя
Лицензирование нашей книги
Эти книги не только бесплатны, но и имеют открытую лицензию! Один и тот же контент, но разные версии (фирменные или нет) имеют разные лицензии, как объяснено:
CC-BY-ND (фирменные версии)
Вам разрешается и поощряется свободное копирование этих версий. Вы можете копировать, распечатывать и распространять их столько раз, сколько захотите. Вы можете загрузить их на свой мобильный телефон, iPad, ПК или флешку. Вы можете записать их на компакт-диск, отправить по электронной почте или загрузить на свой веб-сайт. Единственное ограничение заключается в том, что вы не можете каким-либо образом адаптировать или изменять эти версии учебников, их содержание или обложки, поскольку они содержат соответствующие бренды Siyavula, логотипы спонсоров и одобрены Департаментом базового образования. Для получения дополнительной информации посетите Creative Commons Attribution-NoDerivs 3.0 Непортированный.
Вы можете копировать, распечатывать и распространять их столько раз, сколько захотите. Вы можете загрузить их на свой мобильный телефон, iPad, ПК или флешку. Вы можете записать их на компакт-диск, отправить по электронной почте или загрузить на свой веб-сайт. Единственное ограничение заключается в том, что вы не можете каким-либо образом адаптировать или изменять эти версии учебников, их содержание или обложки, поскольку они содержат соответствующие бренды Siyavula, логотипы спонсоров и одобрены Департаментом базового образования. Для получения дополнительной информации посетите Creative Commons Attribution-NoDerivs 3.0 Непортированный.
Узнайте здесь больше о спонсорстве и партнерстве с другими, которые сделали возможным выпуск каждого из открытых учебников.
CC-BY (версии без торговой марки)
Эти небрендированные версии одного и того же контента доступны для совместного использования, адаптации, преобразования, изменения или дальнейшего развития любым способом, при единственном требовании — отдать должное Сиявуле. Для получения дополнительной информации посетите Creative Commons Attribution 3.0 Unported.
Для получения дополнительной информации посетите Creative Commons Attribution 3.0 Unported.
Структура атома — Научные заметки 9 класса
Открытие атомов стало революционным началом нового и детализированного мира Науки.Каким бы маленьким ни был атом, внутри него заключено множество важных понятий. Это должным образом объясняется в главе «Структура атома» класса 9. В этой главе вы познакомитесь с такими важными темами, как фундаментальные составляющие атома, различные модели атома, распределение электронов, валентности, атомный номер и массовое число. Итак, давайте начнем и рассмотрим эту тему программы 9 класса CBSE .
Основные составляющие атома
Атом состоит из трех основных частиц, а именно протонов, нейтронов и электронов.Ядро атома содержит протоны и нейтроны, где протоны заряжены положительно, а нейтроны нейтральны. Электроны расположены в самых внешних областях, называемых электронной оболочкой.
Электрон
Дж. Дж. Томсон в 1897 г. обнаружил отрицательно заряженные частицы, испускаемые катодом по направлению к аноду, в эксперименте с катодными лучами. Эти отрицательно заряженных частиц и есть Электроны.
Протоны
Эрнест Гольдштейн в 1886 году обнаружил, что при различных условиях в той же камере анод испускает положительно заряженных частиц, известных как канальные лучи или позже названные протонами.
Нейтроны
Дж. Чедвик открыл субатомную частицу с без заряда и массой, эквивалентной протонам в ядрах всех атомов. Эти нейтрально заряженные частицы — нейтроны.
Атомная структура углерода
Атом углерода содержит шесть протонов, шесть электронов и шесть нейтронов, что делает его массовое число равным 12.
Атомная структура кислорода
Атом кислорода содержит восемь протонов, восемь электронов и восемь нейтронов, что делает его массовое число равным 16.
Атомная структура водорода
Атом водорода (H) содержит только один протон, один электрон и не содержит нейтронов.
Атомная структура гелия
Атом гелия содержит два протона, два электрона и два нейтрона, что делает его массовое число равным 2.
Базовая единица жизни Класс 9 Примечания
Различные модели строения атома
Со времени открытия атомов существует множество теорий, которые были сформулированы многими известными учеными.Упомянутые ниже важные теории о структуре атома в соответствии с главой.
Кредиты: Amritacreate
Модель атома Томсона
Дж. Дж. Томсон предположил, что структура атома подобна структуре рождественского пудинга, где электроны встроены в сферу, как смородина. Он предложил, что:
Он предложил, что:
- Структура атома представляет собой положительно заряженную сферу, в которой заключены электроны
- Атом электрически нейтрален, так как протоны и электроны равны по величине
Недостатки модели Томсона: Томсоновская структура атома не смогла объяснить расположение протонов и электронов в его структуре.
Класс 9: Примечания по работе, энергии и мощности
Кредиты: Аасока
Модель атома Резерфорда
Резерфорд провел эксперимент по бомбардировке альфа-(α)-частицами золотой фольги. Он наблюдал траекторию альфа (α)-частицы после прохождения через атом и сформулировал некоторые постулаты эксперимента, а именно:
- Большая часть пространства в атоме пуста, так как частицы беспрепятственно прошли сквозь золотую фольгу
- Положительно заряженный центр называется Ядро , и вся масса атома находится в центре.
 Частицы отклонились 180 0 после бомбардировки ядра
Частицы отклонились 180 0 после бомбардировки ядра - Электроны вращаются вокруг центра по определенной траектории
- Размер ядра мал по сравнению с общим размером атома
Это были постулаты, высказанные Резерфордом с использованием эксперимента по рассеянию альфа-(α)-частиц на золотой фольге.
Недостатки модели: Хотя Резерфорд представил совершенно новую модель строения атома, было много недостатков, которые он не смог объяснить, а именно:
- Электроны вращаются по нестабильной траектории и испытывают ускорение, излучая энергию.Когда электроны вращаются, они теряют энергию. Вскоре электроны сколлапсируют в ядро. Эта тенденция сделала бы атом очень нестабильным, в то время как атом был бы очень стабильным
- Структура атома Резерфорда не смогла объяснить концепцию атомного числа, поскольку она объяснила только присутствие протонов в ядре
.
Кредиты: Амритакреат
Модель атома Бора
Бор разработал модель, чтобы преодолеть возражения, выдвинутые моделью Резерфорда.Так, он сформулировал следующие постулаты:
- Атом допускает только дискретное количество орбиталей для электронов, которые вращаются вокруг своей орбиты и составляют внешнюю структуру атома
- При вращении отрицательно заряженные частицы не теряют энергию на этих орбиталях или энергетических уровнях
- Когда электрон перескакивает с одной энергетической оболочки на другую, происходит изменение величины
Модель Бора дает подробное объяснение строения атома и преодолевает возражения, с которыми сталкиваются все другие модели строения атома.2 дает размещение максимального количества электронов в каждой оболочке, n=1, 2, 3, 4 для K=2, L=8, M=18, N=32 . 2 можно рассчитать количество электронов на любой оболочке.
2 можно рассчитать количество электронов на любой оболочке.
Валентность
Следующим важным понятием в наших заметках о строении атома является понятие валентности. Отрицательно заряженные частицы, присутствующие во внешней оболочке, называются валентными электронами. Эти валентные электроны отвечают за валентность атома.
Валентность – это склонность атома реагировать с другими атомами того же или различных элементов. Атомы, заполняющие крайние пути, проявляют химическую активность по отношению к другим валентным электронам.Эта реакционная способность отвечает за образование молекул между двумя или более атомами.
Валентность становится нулевой для атома, когда внешние границы имеют восемь электронов или не теряют ни одного электрона. Частица с восемью электронами на самой внешней оболочке представляет собой октет, и эти молекулы в основном инертны по своей природе.
Магний (Mg) имеет конфигурацию (2, 8 и 2), , поэтому валентность два . Кислород (O) (2, 8 и 6) имеет валентность две , поскольку количество электронов, которое он может получить, равно двум для достижения упакованного внешнего энергетического уровня.Точно так же Гелий (Не) имеет 2 электрона во внешней оболочке, Неон (Ne) (2, 8 и 8) имеет восемь электронов во внешней оболочке. Следовательно, они не проявляют никакой химической активности.
Кислород (O) (2, 8 и 6) имеет валентность две , поскольку количество электронов, которое он может получить, равно двум для достижения упакованного внешнего энергетического уровня.Точно так же Гелий (Не) имеет 2 электрона во внешней оболочке, Неон (Ne) (2, 8 и 8) имеет восемь электронов во внешней оболочке. Следовательно, они не проявляют никакой химической активности.
Примеры химии в повседневной жизни
Атомный номер (Z)
Ядро атома состоит из протонов , а атомный номер равен числу протонов, присутствующих в одном атоме элемента.Поскольку атом электрически нейтрален, количество протонов и электронов одинаково. Обозначение Z обозначает атомный номер. Атомный номер водорода равен единице, поскольку он имеет только один протон.
Понимание этих основных моментов структуры атома будет полезно для вас-
Количество протонов в атоме = Атомный номер (Z)
Количество электронов, присутствующих в атоме = Атомный номер (Z)
Количество нейтронов = Массовое число (A) — Атомный номер (Z)
Массовый номер (A)
Массовое число является мерой общего числа протонов и нейтронов в ядре атома. Обозначение A указывает на массовый номер . Обозначение N означает общее число нейтронов .
Обозначение A указывает на массовый номер . Обозначение N означает общее число нейтронов .
Массовое число = Атомный номер + Количество нейтронов в ядре
А = Z + №
Массовое число
также называют нуклонным числом.
Изотопы и изобары
Изотопы и изобары — важные понятия, которые вы должны понимать, чтобы лучше понять главу.
Изотопы
Атомы одних и тех же элементов с одинаковым атомным номером и разными массовыми числами. Водород имеет три изотопа: протий, дейтерий, тритий.
Примеры:
Изобары
Атомы разных молекул с одинаковым массовым числом. Например, в кальции с атомным номером 20 и аргоне с атомным номером 18 массовое число обоих этих элементов равно 40. Это показывает, что общее число нуклонов в атомах одинаково.
Примеры:
Важные вопросы и ответы
Q1. Назовите свойства электронов, протонов и нейтронов.
Соль:
| Собственность | Электроны | Протоны | Нейтроны |
| Плата | Отрицательно заряженный | Положительно заряженный | Бесплатно |
| Аффинити | Притягивается к положительно заряженным | Притягивается к отрицательно заряженным | Не привлекайте ни положительное, ни отрицательное |
| Масса | Масса пренебрежимо мала | 1 а.м.у | 1 час ночи |
| Местоположение | Вне ядра | Внутри ядра | Внутри ядра |
Q2. Опишите ограничения модели атома Дж. Дж. Томсона.
Дж. Томсона.
Sol: Согласно этой модели, электроны полностью погружены в положительно заряженные сферы. Но эксперименты показали, что протоны присутствуют только в центре атома, а электроны распределены вокруг ядра атома.
Q3. Укажите ограничения модели атома Резерфорда.
Sol: Согласно этой модели, электроны вращаются по круговой орбите вокруг ядра. Любая такая частица, вращающаяся вокруг ядра, претерпевала бы ускорение и излучала бы энергию. Вращающийся электрон потерял бы свою энергию и в конце концов упал бы на ядро, атом был бы крайне нестабилен. Хотя атомы достаточно стабильны.
Q4. Опишите модель атома Бора.
Sol: проверьте следующие утверждения:
- Атом имеет ядро в центре.
- Отрицательно заряженные электроны вращаются вокруг ядра.
- Атомы ядра содержат различные орбиты электронов.
- Электроны не излучают энергию при вращении по отдельным орбитам
- Эти орбиты или оболочки обозначаются буквами K,L,M,N или цифрами 1,2,3,4.

Q5. Приведите сравнение всех предложенных моделей атома, приведенных в этой главе.
Соль:
| Томсон | Резерфорд | Бор |
| Сфера заряжена положительно. | Положительно заряженная сфера в центре называется ядром. | Положительный заряд в центре называется ядром. |
| Электроны беспорядочно разбросаны по всей сфере. | Электроны вращаются вокруг ядра по орбитам. | Электроны вращаются по дискретным орбитам и не излучают энергию. |
| Положительный заряд = Отрицательный заряд. Атом электрически нейтрален. | Размер ядра очень мал по сравнению с размером атома. | Орбиты обозначались как энергетические оболочки буквами К, Л, М, Н или цифрами 1,2,3,4. |
Модель Томсона атома
Кредиты: Britannica
Резерфордская модель атома
Кредиты: COCC
Модель атома Бора
Кредиты: Classnotes
Таким образом, мы надеемся, что этот блог о структуре атома поможет вам лучше понять программу 9 класса по естественным наукам . Вы также можете обратиться к нашим экспертам Leverage Edu за помощью в принятии важных карьерных решений.
Вы также можете обратиться к нашим экспертам Leverage Edu за помощью в принятии важных карьерных решений.
Извините! — Страница не найдена
Пока разбираемся, возможно, поможет одна из ссылок ниже.
Домой
Назад
- Класс
- Онлайн-тесты
- Ускоренный онлайн-курс JEE
- Двухлетний курс ЕГЭ 2021
- Класс
- Онлайн-курс NEET
- Серия онлайн-тестов
- Фонд CA
- CA Промежуточный
- Финал CA
- Программа CS
- Класс
- Серия испытаний
- Книги и материалы
- Испытательный зал
- Умный взломщик BBA
- Обучение в классе
- Онлайн-коучинг
- Серия испытаний
- Интеллектуальный взломщик IPM
- Книги и материалы
- ГД-ПИ
- CBSE класс 8
- CBSE класс 9
- CBSE класс 10
- CBSE Класс 11
- CBSE Класс 12
- Обучение в классе
- Онлайн-классы CAT
- Серия тестов CAT
- МВА Жилой
- Умный взломщик CAT
- Книги и материалы
- Онлайн-классы без CAT
- Серия испытаний без CAT
- Испытательный зал
- ГД-ПИ
- Обучение в классе
- Серия испытаний
- Гражданские интервью
- Класс
- Онлайн-классы
- Серия испытаний SSC
- Корреспонденция
- Практические тесты
- Электронные книги SSC
- Пакет исследований SSC JE
- Класс
- RBI класс B
- Серия тестов банка
- Корреспонденция
- Банковские электронные книги
- Банк ПДП
- Онлайн-коучинг
- Коучинг в классе
- Серия испытаний
- Книги и материалы
- Класс
- Программа моста GRE
- Онлайн-коучинг GMAT
- Консультации по приему
- Коучинг GMAT в классе
- Стажировка
- Корпоративные программы
- Студенты колледжа
- Работающие специалисты
- Колледжи
- Школы
Руководство для начинающих по английскому языку для 9 класса
Все о руководстве для начинающих по английскому языку для 9 классов
9 класс — важный год для изучающих английский язык. Это первый год этапа 5. В этом году учащиеся выходят за рамки базовых навыков чтения и базового письма и переходят к анализу сложных текстов и разработке сложных продолжительных расширенных эссе.
Это первый год этапа 5. В этом году учащиеся выходят за рамки базовых навыков чтения и базового письма и переходят к анализу сложных текстов и разработке сложных продолжительных расширенных эссе.
Наряду со все более сложными текстами учащиеся должны начать думать и обсуждать методы более высокого порядка. При ответе учащиеся должны будут обсудить свои выводы более подробно, уделяя особое внимание выработке устойчивых, последовательных ответов.
Мы составили это руководство, чтобы помочь учащимся 9-го класса добиться успеха и справиться с этими трудностями.
С какой проблемой номер 1 сталкиваются ученики 9 класса?
Нарушение круиз-контроля.
Учащиеся 9-х классов сталкиваются со многими проблемами, но первопричина всех этих проблем часто сводится к одному и тому же.
Основная проблема, с которой сталкиваются учащиеся 9-х и 10-х классов, — чувство самодовольства.
9-й год и 5-й этап должны быть временем для закрепления и овладения существующими навыками.

Ученикам часто кажется, что 9-й и 10-й классы не в счет, и они перестают настаивать.Студенты очень легко и часто теряют концентрацию на этапе 5 и теряют позиции, полагая, что английский — это просто одно и то же.
Вместо этого 9-й класс — это место, где учащиеся должны развивать свой существующий набор навыков и готовиться к испытаниям английского языка в старших классах.
Что в руководстве?
Это руководство представляет собой исчерпывающий обзор навыков, которые вам необходимо развить, чтобы стать лучшим 9-м классом.
В ней мы затронем следующие темы:
- Как делать и писать заметки
- Анализ текста в 9 классе
- Как анализировать художественную прозу
- Как анализировать поэзию
- Как анализировать Шекспира
- Как анализировать пленку
- Как анализировать изображения и визуальную информацию
- Как анализировать нехудожественную прозу
- Составление ответов в 9 году
- Как писать убедительные эссе
- Как писать творческие ответы
- Как писать речи и презентации
- Экзаменационные навыки 9 класса
Как видите, в 9-м классе есть немало областей, которые вам нужно развивать.
Чего мне ожидать в 9-м году?
В 9-м классе вы можете рассчитывать на более сложные тексты. Это будут как более длинные романы, так и короткие рассказы, затрагивающие более сложные моральные или социальные проблемы.
Поэзия, с которой вы столкнетесь, будет более сложной, а визуальные тексты, такие как фильмы, потребуют от вас более глубокого анализа.
Виды оценочных заданий, с которыми учащиеся сталкиваются на этапе 5 (этап 5 относится к тому, как Управление по стандартам образования Нового Южного Уэльса относится к требованиям к обучению 9 и 10 классов), требуют, чтобы вы сделали большой шаг вперед, если хотите получить оценки. .
Наконец, ваши ответы должны быть длиннее, более подробно обсуждать вещи и обсуждать более сложные идеи.
Давайте посмотрим, что это значит для вас.
Какие навыки мне нужно развивать в 9 классе?
Чтобы преуспеть в решении этих новых задач, вам необходимо развивать и совершенствовать свои навыки английского языка.
Давайте посмотрим, какие навыки вам нужно развить.
Приближение к методам более высокого порядка
Начиная с 9-го класса, вам нужно будет определять, рассматривать и обсуждать литературные приемы более высокого порядка.
Вам нужно будет определить, когда композиторы используют такие вещи, как сарказм, пародия или символизм. Вам нужно будет понять, как эти техники создают смысл и чего композиторы пытаются достичь, используя их.
Обдумывание тем и полных текстов
Вам нужно будет подумать об авторском и текстовом контексте, а также о влиянии, которое он оказывает на смысл текста. Вам нужно будет обдумать, как ваш собственный контекст влияет на то, как вы смотрите на текст.
Это означает спросить себя: «Как мой опыт повлиял на мою точку зрения на этот текст?»
Развитие грамматики и навыков письма
Когда вы будете обсуждать более сложные идеи, вам придется использовать более сложные грамматические конструкции для их воплощения.
Важно, чтобы вы уделяли особое внимание грамматике в 9-м классе, чтобы у вас вырабатывались хорошие привычки и не закреплялись плохие.
Кроме того, вам необходимо тщательно структурировать абзацы.
Например, чтобы передать сложные идеи и обсудить связи между, скажем, текстом, использованием в нем приемов и его контекстом, вам потребуется использовать переходные фразы, чтобы объединить ваши идеи и обсуждение.
Написание устойчивых ответов
Чем сложнее ваше обсуждение текстов и идей, тем длиннее будут ваши ответы.
При составлении ответов от вас ожидают формальных, информативных и убедительных эссе, а не коротких ответов и абзацев.
Чтобы сделать это эффективно, вам необходимо развить навыки работы с указателями — используя тезисы, тематические предложения, утверждения-ссылки и ключевые слова — чтобы помочь вашим читателям ориентироваться в идеях, которые вы обсуждаете.
Изучение и развитие навыков написания сочинений в 9-м классе является важным шагом к написанию ясных, проницательных и лаконичных текстов в 12-м классе.
Организация и учебные привычки
Если вы собираетесь успешно развивать вышеперечисленные навыки, вам необходимо убедиться, что у вас есть всесторонняя и эффективная привычка к обучению.
Знания и навыки не просто материализуются, они являются результатом постоянного обучения, применения и практики!
Как вы, наверное, знаете, английский — не единственный предмет, сложность которого в 9-м классе возрастает. Большинство других предметов тоже.
Однако природа английского языка, многократное чтение и просмотр длинных текстов, требует большего распределения времени. Важно, чтобы вы планировали достаточное время для учебы и придерживались его, чтобы выработать хорошие привычки.Английский будет занимать больше времени по мере вашего продвижения в школе.
Важным навыком, который нужно развивать и совершенствовать в 9-м году жизни, является ведение заметок. Вы должны быть очень компетентны в выявлении важной информации, записи ее для последующего использования в учебных заметках, а затем использовании этих заметок для подготовки ответов или подготовки к экзаменам.
Матричный метод TM для изучения английского языка поможет учащимся развить навыки, которые им необходимо развивать:
Что вы будете записывать в свои учебные заметки? Ваш анализ текстов, которые вы поставили для изучения.
Посмотрим, как изменятся требования к текстовому анализу в 9-м году.
Поднимите свои знания английского языка на новый уровень
Учеба не должна прекращаться, потому что ты дома! С помощью Matrix+ мы предоставляем вам четкие и структурированные онлайн-уроки, качественные ресурсы и форумы, где можно задать вопросы преподавателям Matrix и получить обратную связь.
Узнайте больше о нашем онлайн-курсе английского языка Matrix+ прямо сейчас.
Текстовый анализ в 9 классе
Результаты учебного плана NESA Stage 5 указывают на то, что учащимся необходимо определить более сложные методы в своем анализе, а также учитывать внешние по отношению к тексту вещи, такие как контекст и аудитория.
Это подготовит их к 10 классу английского языка.
Давайте посмотрим, что это значит для вас.
Определение передовых методов
В 9 классе английского языка вам, возможно, потребуется определить литературные приемы более высокого порядка, такие как символизм, расширенная метафора, сатира и пародия.
Вам нужно быть уверенным в обнаружении:
- Ирония
- Сарказм
- Насмешки
- Абстракция
- Значки и символы
- Тон и голос
- Сопоставление
- Преувеличение
- Юмор
- Синтаксис
Углубление чтения
В 9-м классе английского языка вам необходимо учитывать перспективу и структуру текста, а также учитывать такие факторы, как контекст и аудитория.
Вам нужно быть уверенным в идентификации:
- Текстовая структура
- Перспектива и повествовательная точка зрения
- Иконки
- Мифы
- Эстетика
- Назначение
- Голос
- Литературный стиль
- Интертекстуальность, адаптация и аллюзия
- Культурные ценности и предположения
- Ценности, системы ценностей и установки
- Как можно по-разному представлять идеи и использовать их в разных контекстах
Вам также нужно будет подумать о том, как тексты могут вызывать у аудитории чувства:
- Эмпатия
- Симпатия
- Антипатия
- Эстетическая оценка
Какие виды оценок вы можете ожидать?
Чтобы дать вам представление о том, что вас ждет, давайте кратко рассмотрим виды заданий по оценке, с которыми вы можете столкнуться в 9-м классе:
- Вопросы с кратким ответом на понимание : Аналогично предыдущим годам, но тексты будут сложнее, а длина ваших ответов будет увеличиваться с глубиной вашего анализа
- Информативные эссе : эссе, целью которых является информирование читателя о предмете или идее
- Убедительные эссе : эссе, цель которых убедить читателя в обоснованности конкретной точки зрения
- Речи : устные задания, требующие убеждения или информирования аудитории
- Презентации : подобные речам, но представленные с визуальными средствами, такими как реквизит или изображения
- Мультимодальные презентации : Презентации с использованием слайдов PowerPoint или других цифровых визуальных средств
- Подкасты : Тематическая аудиопрезентация в форме эпизода сериализованного шоу подкастов
- Vlogs : запись видеоблога.
 Обычно это личный ответ на проблему или тему в тексте
Обычно это личный ответ на проблему или тему в тексте - Видеоэссе : Похож на видеоблог, но более формален по тону. Видеоэссе включают в себя клипы и изображения, подтверждающие выдвигаемый аргумент
- Размышления : тип письменного задания, в котором вы обсуждаете, как вы подошли к задаче, и взвешиваете, что вы сделали хорошо и плохо. задания на размышление просят вас обсудить, как вы будете совершенствоваться в будущем.
- Рассказы : Рассказы.В 9-м классе от вас ожидают создания рассказов с четкой структурой и хорошо разработанными характеристиками.
- Креативное переосмысление : Фанфики! Форма творческого письма, при которой вы пересказываете аспект или сцену из текста с точки зрения другого персонажа или с другим результатом
- Обоснование : Тип рефлексивного письма, в котором вы объясняете, чего вы пытались достичь с помощью определенного произведения.
 Например, обоснования дают вам возможность объяснить, как вы использовали технику в своем творческом письме.
Например, обоснования дают вам возможность объяснить, как вы использовали технику в своем творческом письме.
.
Как видите, перед вами открывается множество сложных задач. Это создаст трудности, но также настроит вас на 11 и 12 классы.
Примечание об английском языке для этапа 5
Несмотря на то, что мы постарались сделать это Руководство как можно более полным, природа изучения английского языка на уровне 5 означает, что некоторые навыки будут преподаваться в 9-м классе, а другие — в 10-м.
Чтобы убедиться, что вы не пропустили ни одного материала 5-го уровня, вы должны найти время, чтобы прочитать «Руководство для начинающих по английскому языку для 10-го класса», как только вы закончите читать это.
Во-первых, вам нужно знать, как делать заметки
Теперь вы знаете, что вас ждет, и мы начнем обучать вас навыкам, которые вам понадобятся, чтобы стать лучшим 9-м классом.
Поскольку вы не можете писать содержательные ответы без содержательных учебных заметок, мы собираемся показать вам, как делать отличные заметки!
© Matrix Education и www. matrix.edu.au, 2022. Несанкционированное использование и/или копирование этого материала без письменного разрешения автора и/или владельца этого сайта строго запрещено.Выдержки и ссылки могут быть использованы при условии, что Matrix Education и www.matrix.edu.au полностью и четко указаны с соответствующим и конкретным указанием на исходный контент.
matrix.edu.au, 2022. Несанкционированное использование и/или копирование этого материала без письменного разрешения автора и/или владельца этого сайта строго запрещено.Выдержки и ссылки могут быть использованы при условии, что Matrix Education и www.matrix.edu.au полностью и четко указаны с соответствующим и конкретным указанием на исходный контент.
Естественные науки 9 класс
Обзор главы
1 неделя
Эта глава основана на введении в химические уравнения, приведенном в главах 1 и 3 Гр. 8 Материя и материалы.
К этому этапу учащиеся должны знать, что атомы перестраиваются во время химической реакции.Атомы не меняются; меняется только их расположение по отношению друг к другу.
Учащиеся познакомились с диаграммами частиц в Гр. 8, и этот навык будет дополнительно закреплен в этой главе. Мы попытались познакомить учащихся с идеей о том, что химические реакции можно рассматривать по-разному. В конечном счете, они должны уметь составлять химические уравнения, а это очень сложный навык. Начав со словесных уравнений и перейдя к субмикроскопическим представлениям (уравнениям-картинкам), прежде чем переводить последние в символический формат (химические уравнения), мы надеемся построить/подкрепить изучение химических уравнений, а также развить способность учащихся представлять события на субмикроскопический масштаб.
Начав со словесных уравнений и перейдя к субмикроскопическим представлениям (уравнениям-картинкам), прежде чем переводить последние в символический формат (химические уравнения), мы надеемся построить/подкрепить изучение химических уравнений, а также развить способность учащихся представлять события на субмикроскопический масштаб.
2.1 Размышление над химическими уравнениями (0,5 часа)
|
| 8 | 9002 | |||
|
Activity: Drawing Water |
Дополнительно (предлагается) |
2.2 Как представить химические уравнения? (1 час)
|
Задачи |
9002 | |||
|
Activity: Определение различных типов уравнений |
Определение, сортировка и классификация, интерпретация |
Дополнительно (рекомендуется) |
2.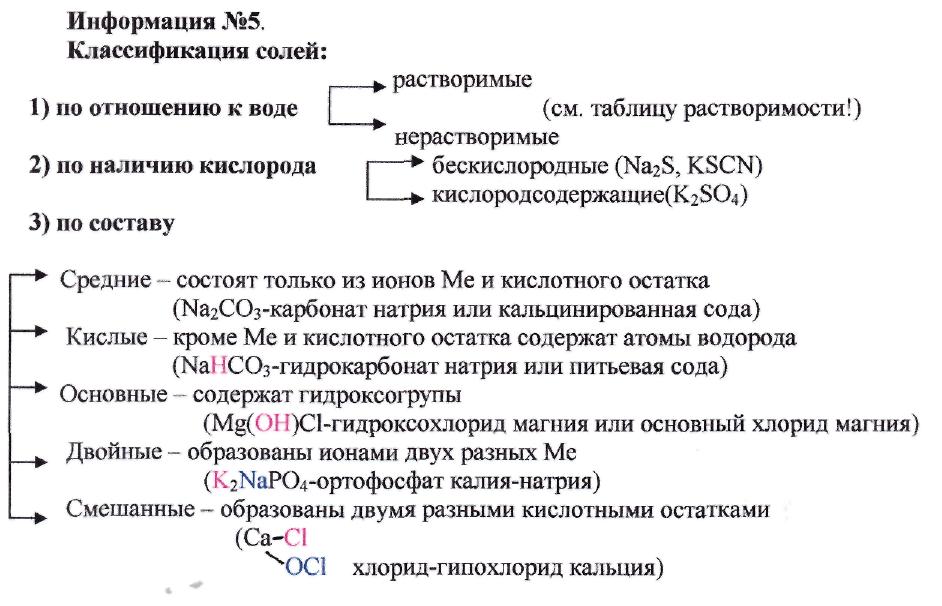 3 Сбалансированные уравнения (1,5 часа)
3 Сбалансированные уравнения (1,5 часа)
|
задачи |
9002 | |||||
|
Активность: когда реакция сбалансирована? |
Интерпретация, написание формул, уравнения балансировки |
9002 | ||||
|
Activity: Magnesium жжение в Oxygen |
Интерпретация, формул письма, уравнения балансировки |
Caps Repained |
||||
|
Активность: железо реагирует с Oxygen |
9002 | 9002 | 9002 |
Caps Repained |
||
|
Активность: Медь реагирует с Oxygen |
Интерпретация, пишу формул, уравнения балансировки, сравнение, рисование |
Предлагаемые CAPS |
В Гр. 8 Материя и материалы мы впервые узнали о химических реакциях . Можете ли вы вспомнить основные идеи о химических реакциях? Вот они снова:
8 Материя и материалы мы впервые узнали о химических реакциях . Можете ли вы вспомнить основные идеи о химических реакциях? Вот они снова:
В этой главе мы собираемся развить эти идеи. Мы сосредоточимся на двух вещах:
Это подготовит нас к последующим главам, в которых мы будем рассматривать различные типы химических реакций.
Однако, прежде чем мы перейдем к химическим реакциям, важно напомнить себе о том, как до сих пор мы думали о химических соединениях.В следующем разделе будет показано, как они все сочетаются друг с другом.
Размышление о химических реакциях
- связь
- реагент
- продукт
- химическая реакция
- макроскопический
- субмикроскопический
- символический
Ученые учатся думать о соединениях на трех разных уровнях:
- макроскопический
- микроскопический
- субмикроскопический
Как молодой ученый, вы уже знакомы с таким мышлением. Три уровня также можно рассматривать как три разных способа представления соединений. Следующее упражнение поможет вам понять, что это значит.
Три уровня также можно рассматривать как три разных способа представления соединений. Следующее упражнение поможет вам понять, что это значит.
ИНСТРУКЦИИ:
Инструкция к этому заданию очень проста: нарисуйте воду. Вы можете использовать пространство ниже для вашего рисунка.
Не давайте никаких дальнейших инструкций, но позвольте учащимся интерпретировать вопрос так, как они хотят. Попросите учащихся показать свои работы. Кто-то может нарисовать пейзаж с водой (плотину или реку), а кто-то может нарисовать стакан или подобный сосуд с прозрачной бесцветной жидкостью внутри.Возможно, один или два нарисуют молекулу воды или химическую формулу воды. Попросите некоторых учащихся перерисовать свои рисунки на доске.
Ваш рисунок может выглядеть как одна из схем ниже. Все они представляют воду. Но какой из них правильный?
Все верно!
Три диаграммы, прежде всего, представляют воду, но они очень отличаются друг от друга.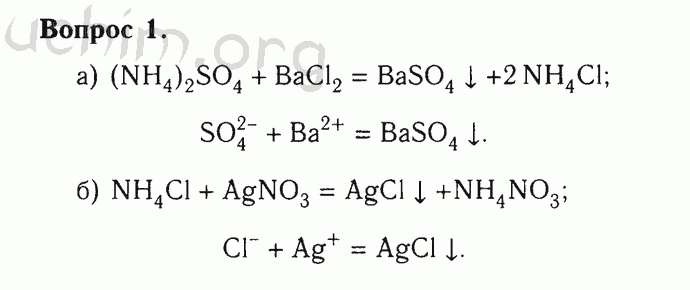 Мы говорим, что это три разных представления одного и того же, а именно воды.
Мы говорим, что это три разных представления одного и того же, а именно воды.
На следующей диаграмме показано, как эти три представления сочетаются друг с другом.
Молекула воды в правом верхнем углу показывает, как могла бы выглядеть частица воды (i). Частицы воды мы не можем видеть глазами, поэтому нам приходится их представлять. Вот почему молекула воды находится внутри мыслепузыря. Мы называем это субмикроскопическим представлением .
Субмикроскопический означает «меньше микроскопического» или «слишком маленький, чтобы можно было увидеть в микроскоп».Иногда полезно подумать, что это то, что мы увидели бы, если бы у нас были специальные «субмикроскопические очки», чтобы «видеть» на атомном уровне!
Стакан с водой показывает, как выглядит вода для наших глаз (ii). Мы называем это макроскопическим представлением , потому что оно наблюдаемо. Это означает, что его можно наблюдать, используя наши чувства, такие как зрение, осязание, слух, вкус или осязание.
Химическая формула слева использует химические символы для обозначения воды (iii).Мы узнали, что химические формулы состоят из символов элементов. Мы можем думать о химических символах и формулах как о химическом «языке», потому что они рассказывают историю. «История», рассказанная формулой H 2 O, заключается в том, что молекула воды состоит из двух атомов H и одного атома O. Формула «H 2 O» представляет собой символическое представление .
Опытные ученые могут легко перемещаться между этими тремя уровнями. Они могут переводить символический язык химических формул в субмикроскопические картинки в своем воображении.Это то, что мы будем практиковать в этой главе.
Прежде чем двигаться дальше, попробуйте другой пример, где вы рисуете 3 разных уровня углекислого газа в пространстве ниже. маркируйте каждый уровень.
Учащиеся могут нарисовать закрытый контейнер с прозрачным газом для макроскопического представления. Они должны написать формулу CO 2 для символического представления. Они должны нарисовать молекулу углекислого газа для субмикроскопического представления следующим образом:
Они должны написать формулу CO 2 для символического представления. Они должны нарисовать молекулу углекислого газа для субмикроскопического представления следующим образом:
Самый маленький в мире фильм из атомов и как его сделали ученые
Как мы представляем химические реакции?
- химическое уравнение
- коэффициент
- индекс
Как бы вы определили химическую реакцию? Запишите некоторые из ваших идей.Следующие слова могут помочь вам сформулировать предложения.
|
реагенты, продукты, связи, перегруппированные, атомы, молекулы, новые соединения |
Предложите учащимся сначала сделать несколько заметок и описать, что, по их мнению, представляет собой химическая реакция. Вы даже можете просто задать им вопрос и получить их определения.
Химическая реакция – это перегруппировка атомов, при которой одно или несколько соединений превращаются в новые соединения.
Все химические реакции могут быть представлены уравнениями и моделями.Некоторым людям химические уравнения могут показаться очень сложными для понимания. Поскольку атомы и молекулы нельзя увидеть, их нужно представить, а это может быть довольно сложно! К счастью, у нас была некоторая подготовка, потому что мы рисовали молекулы со времен Гр. 7.
Всякий раз, когда атомы отделяются друг от друга и рекомбинируются в различные комбинации атомов, мы говорим, что произошла химическая реакция. Атомы не теряются и не приобретаются, они просто перестраиваются.
1. Словесные уравнения
В математических уравнениях мы используем знак равенства (=), например, 2 + 2 = 4, но в научных химических уравнениях мы используем стрелку (→), например, C + O 2 → CO 2 .
Когда мы представляем химическую реакцию словами, мы пишем словесное уравнение . Например, когда газообразный водород реагирует с газообразным кислородом с образованием воды, мы можем записать уравнение реакции следующим образом:
Например, когда газообразный водород реагирует с газообразным кислородом с образованием воды, мы можем записать уравнение реакции следующим образом:
водород + кислород→ вода
Слева от стрелки показана ситуация «до». Эта сторона представляет вещества, которые у нас есть до того, как произойдет реакция. Их называют реагентами . Каковы реагенты этой реакции?
Реагенты: водород и кислород.
Справа от стрелки у нас ситуация «после». Эта сторона представляет собой вещества, которые у нас есть после того, как реакция произошла. Они называются продуктов . Что является продуктом этой реакции?
2. Уравнения изображения
Та же реакция взаимодействия водорода с кислородом также может быть представлена в картинках, называемых субмикроскопическими диаграммами. На приведенной ниже диаграмме показано, что атомы в двух молекулах водорода (H 2 ) и одной молекуле кислорода (O 2 ) слева перестраиваются с образованием двух молекул воды (H 2 O) справа от стрелки. .Атомы водорода — белые кружки, атомы кислорода — красные кружки.
.Атомы водорода — белые кружки, атомы кислорода — красные кружки.
Что это за представление: макроскопическое, субмикроскопическое или символическое?
Субмикроскопический, потому что показывает частицы.
Теперь мы собираемся преобразовать нашу субмикроскопическую картинку в символический конус:
Что является продуктом вышеуказанной реакции? Каковы реагенты вышеописанной реакции? Напишите их формулы.
Продукт H 2 O.Реагенты: H 2 и O 2 .
3. Химические уравнения
Когда мы представляем химическую реакцию в терминах химических формул (символов), она называется химическим уравнением . Химическое уравнение вышеуказанной реакции будет следующим:
2 H 2 + O 2 → 2 H 2 O
Что это за представление: макроскопическое, субмикроскопическое или символическое?
Символический, поскольку использует формулы (символы).
У нас все еще есть реагенты слева и продукты справа.
ИНСТРУКЦИИ:
Заполните следующую таблицу, указав различные типы показанных уравнений, а именно словесные, графические или химические уравнения.
|
Уравнение |
7 | ||
|
Fe + O 2 → Fe 2 О 3 |
|||
|
С 6 Н 12 O 6 + 6O 2 → 6CO 2 + 6H 2 О |
|
Уравнение |
Тип уравнения |
|
Изображение Уравнение |
|
|
углекислый газ + вода → глюкоза + кислород |
Слово уравнение |
|
Fe + O 2 → FE 2 O 3 9002 |
9103 |
|
Уравнение изображения |
|
|
C 6 H 12 o 6 + 6O 2 → 6CO 2 + 6H 2 O |
Символическое/химическое уравнение |
ВОПРОСЫ:
Какой процесс представляет собой уравнение углекислый газ + вода → глюкоза + кислород?
Какой процесс представляет уравнение C 6 H 12 O 6 + 6O 2 → 6CO 2 + 6H 2 O?
Когда вы посмотрите на приведенное выше уравнение реакции, вы заметите два типа чисел:
Коэффициенты и индексы означают разные вещи, как вы увидите в следующем разделе.
Коэффициенты и индексы в химических уравнениях
Почему в химическом уравнении воды перед формулой воды (H 2 O) стоит цифра 2? Это связано с тем, что две молекулы H 2 O могут быть получены из двух молекул H 2 и одной молекулы O 2 в нашей реакции.
Числа перед формулами в химическом уравнении называются коэффициентами . Они представляют собой количество отдельных молекул, участвующих в химической реакции.
Вы заметите, что O 2 не имеет коэффициента в приведенной выше реакции. Отсутствие коэффициента означает, что в реакции участвует только одна молекула этого вещества.
В предыдущей главе мы научились интерпретировать химические формулы. Когда мы читаем формулу, нижних индексов говорят нам, сколько атомов определенного элемента находится в одной молекуле этого соединения.
Сбалансированные уравнения
- сбалансированные
- химическая формула
- ржавчина
- тускнеть
Теперь мы узнаем, что это значит, когда реакция уравновешена . Вот снова наша субмикроскопическая картина.
Вот снова наша субмикроскопическая картина.
Когда учащиеся рисуют двухатомную молекулу, два атома должны соприкасаться с , чтобы показать, что они связаны химически, иначе это неправильно.
Подсчитайте, сколько атомов Н находится в левой части реакции. Сколько справа?
Четыре атома Н слева и четыре атома Н справа.
Подсчитайте, сколько атомов О находится в левой части реакции. Сколько справа?
Два атома О слева и два атома О справа.
Вы заметили, что количество и типы атомов одинаковы слева и справа от реакции? Реагенты имеют четыре атома H и два атома O. Продукты имеют четыре атома H и два атома O.
Когда это верно для уравнения реакции, мы говорим, что уравнение уравновешено .
ИНСТРУКЦИИ:
- Изучите приведенное ниже уравнение. Черные атомы — это углерод (С), а красные атомы — это кислород (О).
 Они не всегда обязательно будут этого цвета — это всего лишь представление.
Они не всегда обязательно будут этого цвета — это всего лишь представление. - Ответьте на следующие вопросы.
ВОПРОСЫ:
Что это за представление: макроскопическое, субмикроскопическое или символическое?
Субмикроскопический, потому что показывает частицы.
Напишите символическое представление (химическое уравнение) указанной выше реакции.
Напишите формулы реагентов этой реакции.
Напишите формулу продукта реакции.
Подсчитайте, сколько атомов С находится в левой части реакции.Сколько справа?
Один атом углерода слева и один атом углерода справа.
Подсчитайте, сколько атомов О находится в левой части реакции. Сколько справа?
Два атома О слева и два атома О справа.
Уравновешена ли реакция? Почему ты так говоришь?
Да, реакция уравновешена, потому что в обеих частях уравнения реакции одинаковое количество атомов одного типа.
Теперь, когда мы знаем, как распознавать сбалансированное уравнение, мы научимся его уравновешивать!
Что такое сбалансированное уравнение? Запишите собственное определение.
Либо попросите учащихся записать свои собственные определения, а затем зачитать их классу, либо они могут просто дать ответы добровольно. Вы можете предложить учащимся начать с: Мы говорим, что уравнение уравновешено, когда… Потенциальный ответ: «Мы говорим, что реакция уравновешена, когда общее количество и типы атомов в реагентах равны таковым в продуктах».
Мы собираемся использовать несколько примеров реальных реакций, чтобы научиться балансировать уравнения. В главах, следующих за этой, мы увидим, как эти реакции выглядят в реальной жизни, но сейчас мы просто сосредоточимся на том, как сбалансировать уравнения.
Хлопья магния часто используются в некоторых фейерверках, таких как бенгальские огни, потому что при горении они создают яркие мерцающие искры.
Когда металлический магний горит в кислороде, мы можем написать следующее словесное уравнение для реакции, которая происходит между этими двумя элементами:
магний + кислород → оксид магния
Хлопья магния горят в кислороде в бенгальском огне. http://www.flickr.com/photos/derekskey/321
http://www.flickr.com/photos/derekskey/321
93/
ВОПРОСЫ:
Что является реагентами реакции?
Реагенты: магний и кислород.
Продукт представляет собой оксид магния.
Мы можем преобразовать слово уравнение в химическое уравнение:
Mg + O 2 →MgO
Что это за представление: макроскопическое, субмикроскопическое или символическое?
Символический, поскольку использует формулы (символы).
Уравнение сбалансировано? Если вы не уверены, посчитайте количество атомов каждого типа слева и справа. Возможно, поможет взглянуть на субмикроскопическое представление (диаграмму частиц) реакции:
Вы можете записать свои результаты в таблицу ниже:
|
Количество атомов |
Реактивы |
Продукция |
91 029 Мг |
91 029 |
91 027
Количество атомов
Реактивы
Продукция
Мг
1
1
О
2
1
Каков ваш вывод: сбалансировано ли уравнение? Поясните свой ответ.
Нет, уравнение не сбалансировано, потому что число атомов в реагентах и продуктах неодинаково.
Как же сбалансировать уравнение, описывающее горение магния в кислороде? При балансировке реакций есть одно простое правило:
Вы можете добавлять только те соединения, которые уже есть в уравнении. Это означает, что могут быть изменены только коэффициенты, а не индексы!
Давайте попробуем несколько альтернативных решений. Поможет ли добавление атома O справа, вот так?
Теперь атомы O сбалансированы по обеим сторонам уравнения, но у нас больше нет MgO справа.Мы изменили формулу справа на MgO 2 . Это означает, что мы изменили индекс в формуле. Вы не можете изменить формулу соединения при балансировке химических уравнений.
Спросите учащихся, почему это запрещено. Является ли MgO таким же, как MgO 2 ? Напомните им о более раннем примере H 2 O и H 2 O 2 , которые не были одним и тем же соединением. MgO и MgO 2 не могут быть одним и тем же соединением, потому что у них разные химические формулы.Соотношение атомов Mg и O в этих двух соединениях различно. (Соединения MgO 2 даже не существует, но вам не нужно в это вдаваться.)
MgO и MgO 2 не могут быть одним и тем же соединением, потому что у них разные химические формулы.Соотношение атомов Mg и O в этих двух соединениях различно. (Соединения MgO 2 даже не существует, но вам не нужно в это вдаваться.)
Добавление отдельных атомов в любую часть уравнения также не допускается. Это означает, что следующее уравнение также неверно:
Помните, что мы можем использовать только те химические формулы, которые уже есть в уравнении. Нам нужны два MgO справа, чтобы сбалансировать два O в O 2 . Нам также нужны два Mg слева, чтобы сбалансировать два MgO справа.
Можете ли вы составить это уравнение из шариков или бусинок из пластилина? Когда вы превращаете «реагенты» теста для лепки в «продукты», остаются ли после этого неиспользованные «атомы»?
Нет, нет. Предложите учащимся выполнить это задание и попрактикуйтесь в составлении уравнения, используя сбалансированное число атомов.
Теперь давайте сделаем еще один шаг. Мы собираемся преобразовать наше сбалансированное субмикроскопическое уравнение в символическое химическое уравнение. Напишите сбалансированное уравнение горения магния в кислороде с образованием оксида магния.
Мы собираемся преобразовать наше сбалансированное субмикроскопическое уравнение в символическое химическое уравнение. Напишите сбалансированное уравнение горения магния в кислороде с образованием оксида магния.
Напишите это на доске и еще раз объясните, как уравновешивается уравнение:
2 Mg + O 2 → 2 MgO
Вот несколько важных правил балансировки химических уравнений:
- Когда мы уравновешиваем уравнения реакций, мы можем добавлять коэффициенты ТОЛЬКО к химическим формулам, которые уже есть в уравнении.
- Мы НЕ МОЖЕМ изменять химические формулы любых реагентов или продуктов, изменяя нижние индексы в формуле.
- Мы НЕ МОЖЕМ добавлять другие реагенты или продукты. Это включает добавление отдельных атомов любого из элементов, уже включенных в уравнение реакции.
- Мы НЕ МОЖЕМ удалять реагенты или продукты.
Теперь мы готовы попрактиковаться в балансировке других уравнений реакции.
Когда железо ржавеет, это происходит потому, что металлическое железо вступает в реакцию с кислородом воздуха с образованием оксида железа.
Старая машина с ржавчиной на капоте. http://www.flickr.com/photos/dok1/3513263469/
Фото ржавой бочки крупным планом.http://www.flickr.com/photos/jeua/7217824700/
Уравнение слова следующее:
железо + кислород → оксид железа
Химическое уравнение выглядит следующим образом:
Fe + O 2 → Fe 2 O 3
Уравнение сбалансировано? Нарисуйте субмикроскопическую картину, чтобы помочь вам принять решение.
Диаграмма ученика должна выглядеть так. Им может быть трудно преобразовать уравнения в диаграммы.Помогите им интерпретировать формулы следующим образом: Fe само по себе означает, что есть только один атом железа (Fe). O 2 означает, что должны быть два атома O, соединенные в молекулу. Fe 2 O 3 означает, что два атома Fe и три атома O сгруппированы вместе.
Цвета не важны, если все атомы одного и того же элемента одного цвета. Расположение атомов в «кластере» Fe 2 O 3 также не имеет значения.Поскольку Fe 2 O 3 является ионным соединением, мы обычно не говорим о «молекуле» Fe 2 O 3 . Как и все другие ионные соединения, он состоит из больших кластеров ионов Fe3+ и O 2 — в правильной кристаллической упаковке, простирающейся в трех измерениях, очень похожей на ионную решетку NaCl на рисунке ниже (показанном также в главе 1).
Не рекомендуется упоминать эту информацию здесь, так как она скорее запутает учащихся, чем поможет им лучше понять уравнения балансировки.
Вы также можете использовать таблицу, подобную приведенной ниже:
|
Количество атомов |
Реактивы |
Продукция |
|
Количество атомов |
Реактивы |
Продукция |
|
Fe |
1 |
2 |
|
О |
2 |
3 |
Каков ваш вердикт: сбалансировано ли уравнение? Поясните свой ответ.
Нет, уравнение не сбалансировано, потому что число атомов в реагентах и продуктах неодинаково.
Как сбалансировать реакцию? Три возможности (Планы A, B и C) приведены ниже. Вы должны оценить каждый план и сказать, разрешен он или нет.
План А
|
Внесены изменения |
Разрешено ли это изменение? Да нет? |
Причина |
|
Добавьте один атом Fe на стороне реагента. |
||
|
Заменить O 2 на O 3 в реагентной части уравнения. |
|
Внесены изменения |
Разрешено ли это изменение? Да нет? |
Причина |
|
Добавьте один атом Fe на стороне реагента. |
Да |
Атом железа уже является реагентом. |
|
Замените O 2 на O 3 в реагентной части уравнения. |
Нет |
Изменения формул не допускаются. |
Преобразуйте уравнение изображения выше в химическое уравнение.
Изменились ли какие-либо коэффициенты? Помните, что это разрешено.
Были ли изменены какие-либо формулы или добавлены новые формулы? Помните, что это НЕ разрешено.
Как вы думаете: сработает ли этот план? Поясните свой ответ.
Нет, так как была изменена формула.
План Б
|
Внесены изменения |
Разрешено ли это изменение? Да нет? |
Причина |
|
Добавьте один атом Fe на стороне реагента. |
||
|
Добавьте один атом О со стороны реагента. |
|
Внесены изменения |
Разрешено ли это изменение? Да нет? |
Причина |
|
Добавьте один атом Fe на стороне реагента. |
Да |
Атом железа уже является реагентом. |
|
Добавьте один атом О на стороне реагента. |
Нет |
Добавление отдельных атомов не допускается, если только они уже не участвуют в реакции КАК ОТДЕЛЬНЫЕ АТОМЫ. |
Преобразуйте уравнение изображения в химическое уравнение.
Изменились ли какие-либо коэффициенты? Помните, что это разрешено.
Были ли изменены какие-либо формулы или добавлены новые формулы? Помните, что это НЕ разрешено.
Как вы думаете: сработает ли этот план? Объясните, почему да или почему нет.
Нет, так как добавление формул запрещено.
План С
|
Внесены изменения |
Разрешено ли это изменение? Да нет? |
Причина |
|
Добавьте три атома Fe на стороне реагента. |
||
|
Добавьте две молекулы O 2 на стороне реагента. |
||
|
Добавьте один Fe 2 O 3 со стороны продукта. |
|
Внесены изменения |
Разрешено ли это изменение? Да нет? |
Причина |
|
Добавьте три атома Fe на стороне реагента. |
Да |
Атом железа уже является реагентом. |
|
Добавьте две молекулы O 2 на стороне реагента. |
Да |
Молекула O 2 уже является реагентом. |
|
Добавьте один Fe 2 O 3 на стороне продукта. |
Да |
Fe 2 O 3 уже является продуктом. |
Преобразуйте уравнение изображения в химическое уравнение.
Изменились ли какие-либо коэффициенты? Помните, что это разрешено.
Были ли изменены какие-либо формулы или добавлены новые формулы? Помните, что это НЕ разрешено.
Как вы думаете: сработает ли этот план? Объясните, почему да или почему нет.
Да, потому что ни одно из правил балансировки уравнений не было нарушено.
Какой из трех планов (A, B или C) помог нам сбалансировать уравнение, используя только разрешенные ходы?
Есть ли какие-нибудь другие планы, которые вы можете придумать, чтобы сбалансировать это уравнение?
Учащихся следует поощрять к тому, чтобы они пробовали другие возможности.Они должны прийти к выводу, что реакция, предложенная в плане С, является единственно правильной.
В следующем упражнении мы сбалансируем уравнение, которое намного проще, но мы не собираемся включать все объяснения предыдущего задания.
Вы когда-нибудь замечали, как медные изделия со временем тускнеют?
Одна из этих медных монет потускнела, так как была покрыта черным веществом. http://www.flickr.com/photos/dno1967b/69965
http://www.flickr.com/photos/dno1967b/69965
/
Этот темный слой потускнения является результатом медленной реакции между медью и кислородом с образованием оксида меди.
ВОПРОСЫ:
Напишите уравнение этой реакции. Все слова есть в предложении выше, их просто нужно поместить в правильные места.
Учащиеся должны заполнить ответы следующим образом:
Преобразуйте слово уравнение в химическое уравнение. Вам не нужно балансировать его еще.
Преобразуйте химическое уравнение в уравнение изображения. Это не должно быть сбалансировано.
Рисунок учащегося должен выглядеть следующим образом.Цвета не обязательно должны быть такими же, как показано здесь, но они должны показывать разницу между различными элементами. Если у учащихся нет карандашей разного цвета, они также могут использовать разные узоры, чтобы различать разные атомы.
Теперь перерисуйте уравнение изображения так, чтобы оно было сбалансированным. Помните, что никакие «новые» соединения добавлять нельзя; нам разрешено только рисовать больше молекул, которые уже есть.
преобразовать сбалансированное уравнение изображения в сбалансированное химическое уравнение.
В следующих главах будет больше возможностей написать и сбалансировать химические уравнения.
Доктор Джекилл и мистер Хайд
Резюме и анализ
Глава 8 — Последняя ночь
Резюме
Однажды вечером после ужина Аттерсон мирно сидит у своего камина, когда к нему приходит очень взволнованный и расстроенный мистер Пул.Он предлагает Пулу стакан вина, чтобы успокоить его, и, хотя Пул принимает его, он не пьет его, нерешительно рассказывая Аттерсону о своих опасениях по поводу доктора Джекила. Пул ужасно боится. Он опасается, что имела место «нечестная игра», природу которой он «не осмеливается сказать». При этих словах Аттерсон хватает свою шляпу и шинель, и двое мужчин отправляются дикой, холодной мартовской ночью к дому Джекила. Когда они приходят в покои Джекила, слуга очень осторожно открывает дверь и спрашивает: «Это ты, Пул?» Оказавшись внутри, Аттерсон обнаруживает, что все слуги Джекила «сбились в кучу, как стадо овец», и когда они видят Аттерсона, одна служанка начинает «истерически хныкать». Это дело гораздо серьезнее, чем Аттерсон мог себе представить. Несколько слуг пытаются заговорить, но Пул заставляет их замолчать и ведет Аттерсона через задний сад, предупреждая адвоката, что, если «случайно» Джекил пригласит его в свою личную комнату, , не уходи». Этот совет, наряду с едва сдерживаемым ужасом Пула, нервирует Аттерсона.
Это дело гораздо серьезнее, чем Аттерсон мог себе представить. Несколько слуг пытаются заговорить, но Пул заставляет их замолчать и ведет Аттерсона через задний сад, предупреждая адвоката, что, если «случайно» Джекил пригласит его в свою личную комнату, , не уходи». Этот совет, наряду с едва сдерживаемым ужасом Пула, нервирует Аттерсона.
Двое мужчин подходят к двери кабинета доктора Джекилла в лаборатории. Пул кричит, что Аттерсон здесь, и просит вызвать врача. Странный голос внутри заявляет, что Джекил никого не увидит.Пул вежливо говорит: «Спасибо». Затем, вернувшись на кухню, он спрашивает Аттерсона: «Это был голос моего хозяина?» Аттерсон бледнеет. «Кажется, многое изменилось», — говорит он, пытаясь скрыть свои страхи. Пул тупой. «Изменился», — говорит он, — вряд ли это слово соответствует голосу «Джекилла». Пул говорит, что проработал на Джекила двадцать лет. Голос, который они услышали, был , а не голосом доктора Джекилла. Восемь дней назад, говорит Пул, он услышал, как Джекилл выкрикнул имя Бога.
По мнению Пула, д-р.В то время с Джекилом «убрали», и кто бы ни был в комнате сейчас, это «вещь, известная только небесам».
Аттерсон изо всех сил старается быть рациональным в отношении тайны. По логике, говорит он, если кто-то убил Джекила, почему он все еще там? Затем Пул рассказывает больше о том, кто находится в комнате. «Что бы это ни было, это , — говорит он, — оно ночь за ночью требует какого-нибудь лекарства». Раньше Джекил выпрашивал определенные лекарства, писал свои приказы на листе бумаги и бросал листок на лестницу.Уже неделю на лестнице снова валяются бумаги, закрытая дверь и хныканье. Пул сделал все возможное, чтобы найти точное лекарство, но что бы он ни привез, это не было «нужным лекарством». «Это» всегда говорит о том, что Пул принес что-то «нечистое», и поэтому Пул продолжает получать приказы отправиться с очередным поручением в еще один магазин. «Этот препарат очень нужен», — говорит Пул Аттерсону.
Аттерсон просит некоторые из этих заметок, и Пул находит одну, скомканную в одном из карманов. На первый взгляд, записка кажется просто формальной просьбой — ничего лишнего — с просьбой к фармацевту поискать лекарство «с самой тщательной тщательностью». Расходы не учитываются, подчеркивается в записке, и есть ощущение срочности: «Важность этого для доктора Джекила трудно переоценить». А затем в нацарапанной приписке есть: «Ради Бога, найдите мне немного старого [наркотика]».
На первый взгляд, записка кажется просто формальной просьбой — ничего лишнего — с просьбой к фармацевту поискать лекарство «с самой тщательной тщательностью». Расходы не учитываются, подчеркивается в записке, и есть ощущение срочности: «Важность этого для доктора Джекила трудно переоценить». А затем в нацарапанной приписке есть: «Ради Бога, найдите мне немного старого [наркотика]».
Аттерсон, наконец, должен признать, что это действительно темное дело. Более чем туманно, говорит Пул: «Я видел его », добавляет он, имея в виду того, кто прячется за дверью Джекила.Однажды, по словам Пула, он вошел в большую комнату прямо под личной комнатой Джекила, и там, копаясь среди каких-то ящиков, было существо, которое так испугалось, увидев Пула, что вскрикнуло «и взметнулось наверх». Если этот был Джекилом, почему он запустился? Почему он «кричал, как крыса»? И почему оно было в маске?
Когда-либо рациональный адвокат-сыщик, Аттерсон пытается объяснить Пулу, что, по его мнению, Джекил «охвачен одной из тех болезней, которые мучают и уродуют страдающего. Он надеется, что безумно востребованный препарат является доказательством того, что Джекилл верит в возможность «полного выздоровления».
Он надеется, что безумно востребованный препарат является доказательством того, что Джекилл верит в возможность «полного выздоровления».
Несмотря на рациональные объяснения Аттерсона, Пул не убежден: «Эта вещь не была моим хозяином… это был скорее гном… вы думаете, я не знаю своего хозяина?… эта штука никогда не была Доктором
Джекил — Бог знает, что это было, но это никогда не был Доктор Джекил». Он непреклонен: «По вере моего сердца… . . убийство было совершено.»
Аттерсон говорит, что если Пул убежден, то у Аттерсона нет альтернативы: он считает своим долгом выломать дверь Джекилла, и Пул может использовать топор, который находится в операционной, а Аттерсон воспользуется каминной кочергой.Однако прежде чем начать, они признаются друг другу, что оба верят, что Хайд находится в комнате и что это он убил Джекила. Они вызывают Брэдшоу, одного из слуг Джекила, и просят его и мальчика следить за лабораторией на другой стороне площади. Затем они устанавливают свои часы. Через десять минут они штурмуют красную деревянную дверь личной комнаты доктора Джекилла.
Через десять минут они штурмуют красную деревянную дверь личной комнаты доктора Джекилла.
По прошествии нескольких минут в комнате Джекила становится тихо, пока все, что они могут слышать, это мягкие, легкие шаги, сильно отличающиеся от тяжелых скрипучих шагов Джекила, расхаживающих взад и вперед.«Болезненная совесть, — шепчет Пул, — кровь пролилась». По истечении десяти минут на ближайшем столе ставится свеча, чтобы дать им больше света. Затем Аттерсон выкрикивает: «Джекилл, я требую встречи с тобой».
Голос, который отвечает Аттерсону, умоляет: «Ради Бога, помилуй!» Аттерсон ошеломлен: это не голос Джекила. Он принадлежит Хайду. Мгновенно он кричит Пулу: «Долой дверь!» Пул четыре раза ударяет топором по крепкой красной двери, и каждый раз внутри раздаются унылые звериные крики.На пятый раз замок лопается, и дверь проваливается внутрь. Сцена внутри странная и неуместная. В очаге мерцает тихий огонь, поет чайник, на рабочем столе аккуратно расставлены бумаги, разложены к чаю. И все же посреди этой уютной сцены тело мужчины лежит лицом вниз, ужасно скрюченное и все еще дергающееся. Тело действительно похоже на карлика, одетого в одежду, слишком большую для него, одежду, которая подошла бы Джекилу по его большому росту.Понятно, что вся жизнь ушла, несмотря на то, что мышцы продолжают непроизвольно подергиваться. В одной руке остатки раздавленного флакона. Аттерсону это кажется явным случаем самоубийства. Он строго говорит Пулу, что они пришли слишком поздно, чтобы спасти или наказать Хайда. Теперь остается только одна задача: они должны найти тело Джекила.
И все же посреди этой уютной сцены тело мужчины лежит лицом вниз, ужасно скрюченное и все еще дергающееся. Тело действительно похоже на карлика, одетого в одежду, слишком большую для него, одежду, которая подошла бы Джекилу по его большому росту.Понятно, что вся жизнь ушла, несмотря на то, что мышцы продолжают непроизвольно подергиваться. В одной руке остатки раздавленного флакона. Аттерсону это кажется явным случаем самоубийства. Он строго говорит Пулу, что они пришли слишком поздно, чтобы спасти или наказать Хайда. Теперь остается только одна задача: они должны найти тело Джекила.
Они обыскивают все крыло, но ничего не находят: «нигде не было никаких следов Генри Джекила, ни мертвого, ни живого». Они идут в секционную и находят ключ Хайда, сломанный пополам и ржавый.Тайна остается. Они снова поднимаются и осматривают мертвое тело Хайда, а затем начинают осматривать химическое оборудование Джекила. Пул указывает Аттерсону на кучу «белой соли», за которой Джекил отправил его с поручениями.
Чайник внезапно закипает и пугает их; Аттерсон берет благочестивое литературное произведение и приходит в ужас от богохульств, написанных на полях. «Шеваль», зеркало в полный рост, озадачивает обоих мужчин. «Этот стакан видел некоторые странные вещи», — шепчет Пул.
Осматривая рабочий стол Джекила, Аттерсон замечает большой конверт с его именем и распечатывает его; несколько корпусов падают на пол.Первое, что он читает, это завещание, очень похожее на то, которое Джекилл оставил Аттерсону ранее. Однако на этот раз бенефициаром Джекила назначен Аттерсон, а не Хайд. На мгновение Аттерсон ошеломлен. Зачем Джекилу составлять новое завещание? Аттерсон знает, что в прошлом он чрезмерно придирался к Джекилу и делал ему выговоры. Наверняка Джекилл злился на Аттерсона за его требовательность. Но почему Джекил сделал Аттерсона своим бенефициаром?
Затем Аттерсон изучает другой лист бумаги.Крича на Пула, он с радостью узнает почерк доктора и дату вверху записки: Джекилл «был жив и сегодня здесь», — плачет он. Конечно, думает Аттерсон, доктор должен быть жив; возможно, он сбежал. С большим беспокойством он решает прочитать следующее вложение.
Сообщение короткое. Джекил исчез при обстоятельствах, которые он мог «предвидеть». Однако его конец, как он опасается, неизбежен. Он просит Аттерсона сначала прочитать записку доктора Лэниона, поскольку Лэнион сказал Джекилу, что его записка теперь находится у Аттерсона.Если после прочтения повествования Лэньона остаются вопросы без ответов, Аттерсон должен прочитать большой запечатанный пакет, содержащий «признание» Джекила.
Аттерсон поворачивается к Пулу и просит ничего не говорить об этом запечатанном пакете; возможно, они еще смогут спасти репутацию Джекила. Взглянув на часы, он видит, что уже десять часов. Он пойдет домой, прочтет документы, вернется до полуночи, а потом пошлют за полицией.
Анализ
Глава 8 функционирует как, пожалуй, самая традиционная повествовательная глава в романе.В большинстве других глав представлено происшествий : «История [или происшествие] у двери», «Происшествие с письмом», «Замечательное происшествие с доктором Ланьоном» и «Происшествие у окна»; другие отделения также дают отчеты о завещаниях, о том, что сообщается в газетах, в «Отчете» доктора Ланиона и, наконец, в собственном «Заявлении» доктора Джекилла. Напротив, эта глава в своих повествовательных последовательностях пролетает с такими разнообразными действиями, как сбор сил в доме Джекила (и обратите внимание, как напуганы все слуги: некоторые, как горничная, впадают в истерику; точно так же все стоят «сбившись в кучу» как стадо овец»).Они в ужасе от того, за что выступает мистер Хайд, и боятся, что он может появиться. Затем в быстрой последовательности происходит взлом двери Джекила, обнаружение мертвого тела Эдварда Хайда, лихорадочные поиски доктора Джекила, обнаружение нового завещания, новой записки и последнее заявление доктора Джекила. . Другими словами, в то время как многие из других глав посвящены только одному отдельному происшествию, эта глава переполнена множеством происшествий.
Начало главы довольно затянуто, потому что обезумевший Пул недостаточно образован, чтобы убедить Аттерсона в серьезности странных событий, происходящих в доме доктора Уайта.Лаборатория Джекила. Следует отметить долгий и трудоемкий метод, с помощью которого Аттерсон окончательно убеждается. То есть каждый раз, когда Пул предлагает некоторую информацию, Аттерсон может предложить какое-то рациональное объяснение; он видит в верном Пуле всего лишь суеверного слугу.
Аттерсон еще не готов действовать, но когда Пул показывает Аттерсону звук голоса за дверью, Аттерсон признает, что изменение действительно произошло. Затем, когда Аттерсону рассказывают о том, что восемь дней назад Пул услышал крик отчаяния, о непрекращающемся плаче день и ночь, о отчаянной потребности в каких-то химикатах и лекарствах, о мимолетном взгляде странного человека в лаборатории, о плачущем о кажущейся потерянной душе и о карликовой фигуре, которую Пул считает Эдвардом Хайдом, Аттерсон, наконец, готов действовать.
Выломав дверь и увидев мертвеца (самоубийцу) в лаборатории, Аттерсон и мы, читатели, по-прежнему думаем, что мертвец — это Эдвард Хайд, хотя «одежда была слишком велика для него, одежда о величии доктора». Кроме того, недоумение Аттерсона по поводу того, почему такой злой человек покончил жизнь самоубийством, добавляет загадочности. Затем тайна двойственности усиливается предположением Аттерсона, что Хайд убил доктора Джекила. Поиски тела Джекила до сих пор оставляют читателя в напряжении по поводу дихотомии или двойственности Джекила/Хайда, особенно когда поиски доктора Хайда продолжаются.Тело Джекила, конечно, бесполезно: «Нигде не было никаких следов Генри Джекила, ни мертвого, ни живого».
Обнаружение сломанного ключа и ржавых «трещин» (дверей или отверстий под ключ) позволяет предположить, что рациональные действия Джекила позволили ему обустроить свои жилые помещения так, чтобы Хайд не мог выйти через черный ход. Он не мог выйти через парадную дверь, потому что после убийства сэра Дэнверса его бы схватили или, по крайней мере, донесли бы слуги.Таким образом, даже в самый безумный конец своей жизни Джекилл сохраняет достаточно своего прежнего рационального «я», чтобы держать Хайда в рамках.
Когда Аттерсон и Пул осматривают лабораторию доктора Джекила, обнаруживаются новые доказательства двойственности Джекилла и Хайда. Например, они находят благочестивую книгу, которую Джекил очень уважал, «отмеченную его собственной рукой поразительными богохульствами». Но, конечно, Аттерсон здесь заблуждается. Если бы он вспомнил анализ почерка своего ассистента, мистера Геста, — что почерк Хайда и Джекила был практически одинаковым, за исключением немного другого наклона, — то он бы понял, что вульгарные и богохульные примечания были сделаны Хайдом, а не Джекиллом, и тем не менее они одинаковы, что, по иронии судьбы, подчеркивает двойственность человека.
Вся тайна достигает своего апогея в конце этой главы с открытием нового завещания доктора Джекила, что делает Габриэля Джона Аттерсона единственным бенефициаром Джекила. Имя Эдварда Хайда вычеркнуто. Аттерсона смущает то, что мерзкий, злой Хайд явно был там, в лаборатории, видел изменение в завещании, но ничего не сделал. Более того, судя по дате краткой заметки — датированной тем днем — Аттерсон совершенно сбит с толку из-за осознания того, что ранее в тот же день Джекилл был еще жив.Наконец, в записке, которую Джекил оставил Аттерсону, снова появляется слово «исчез»: «Когда это попадет в ваши руки, я исчезну». Это же слово появилось в первоначальном завещании Джекила, а также в инструкциях доктора Лэньона Аттерсону, и теперь оно снова появляется в этом письме. Поэтому Аттерсон в полном замешательстве. И поскольку последние две главы являются «документами», и мы больше не видим и не слышим Аттерсона, мы можем только догадываться о том, как эта странная информация от двух его ближайших друзей повлияет на него.
.

 ) и Cu
) и Cu \(1\). Самородная сера
\(1\). Самородная сера

